题目内容
17.下列措施对增大反应速率明显有效的是( )①Na与水反应时,增大水的用量
②做铝与氧气反应的实验时,将铝片改为铝粉
③Zn与稀H2SO4反应式,滴加少量CuSO4溶液
④常温下Fe与稀硫酸反应制取氢气时,改用浓硫酸
⑤用H2O2制取O2时,加入少量MnO2.
| A. | ①②④ | B. | ②③④ | C. | ①④⑤ | D. | ②③⑤ |
分析 ①改变纯液体的量对反应速率无影响;
②增大固体物质的接触面积能够加快反应速率‘
③形成原电池能加快反应速率;
④浓硫酸具有强氧化性,Fe与浓硫酸反应不生成氢气;
⑤催化剂能够加快反应速率.
解答 解:①因水为纯液体,则改变水的量对反应速率无影响,故错误;
②将Al片改成Al粉,增大了反应物的接触面积,所以能使反应速率加快,故正确;
③Zn置换出硫酸铜溶液中的Cu,与稀硫酸构成Cu、Zn原电池,从而加快反应速率,故正确;
④因浓硫酸具有强氧化性,Fe与浓硫酸反应不生成氢气,则不会加快生成氢气的速率,故错误;
⑤在过氧化氢分解中,MnO2能够作催化剂,催化剂能够加快反应速率,故正确;
故选D.
点评 本题考查影响化学反应速率的因素,明确纯固体、纯液体的用量改变对反应速率无影响,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列说法不正确的是( )
| A. | 在熔融电解质中,O2-向正极定向移动 | |
| B. | 通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-═4CO2↑+5H2O | |
| C. | 通入空气的一极是正极,电极反应为:O2+4e-═2O2- | |
| D. | 电池的总反应是:2C4H10+13O2═8CO2+10H2O |
14.标准状况下,2.24L HCl气体溶于100g水中,溶液密度为ρ g•mL-1,所得溶液中溶质的物质的量浓度为( )
| A. | 1mol•L-1 | B. | $\frac{100ρ}{103.65}$mol•L-1 | ||
| C. | $\frac{ρ}{103.65}$mol•L-1 | D. | 无法确定 |
12.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙烯的分子式:C2H4 | ||
| C. | 乙酸的结构简式:C2H2O2 | D. | 丙烷分子的球棍模型是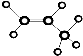 |
2.香兰素的结构简式为: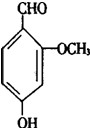 它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
 它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )| A. | 可与银氨溶液反应 | B. | 可与氢氧化钠溶液反应 | ||
| C. | 可与浓溴水发生取代反应 | D. | 分子中所有原子都在同一平面 |
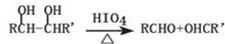
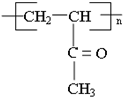 .
.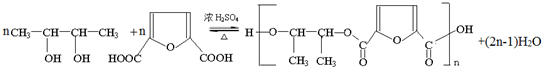 .
.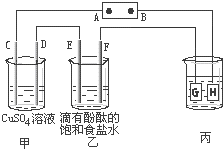 如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.