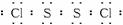题目内容
S2Cl2是一种金黄色易挥发的液体(熔点:-76℃,沸点:138℃),易水解,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质.向熔融的硫中通入干燥、纯净的Cl2即可生成S2Cl2.下图是实验室制备S2Cl2的装置(夹持装置、加热装置均已略去).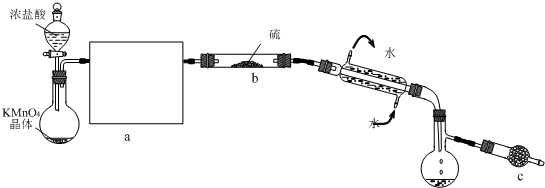
请回答下列问题:
(1)写出仪器C的名称:
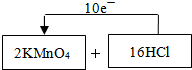
(2)该实验将浓盐酸滴入高锰酸钾晶体可以快速产生氯气,请写出该反应的化学方程式:
(3)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以下滴,经检查分液漏斗活塞没有堵塞,你认为应采取的措施是:
(4)①在下列方框中画出图a中所缺装置图,并注明相关试剂的名称.

②图d装置中应放置的试剂为碱石灰,其作用是
(5)某同学通过查阅资料发现:实验室常利用软锰矿(主要成分为MnO2和一些不溶性杂质)制取KMnO4晶体,其反应原理如下:3MnO2+6KOH+KClO3
3K2MnO4+KCl+3H2O,3MnO2-4+4H+=2MnO-4+MnO2↓+2H2O.请设计由软锰矿制备KMnO4晶体的实验步骤:
①将软锰矿与固体KOH和KClO3在高温下共熔,发生反应;②

请回答下列问题:
(1)写出仪器C的名称:
冷凝管
冷凝管
.(2)该实验将浓盐酸滴入高锰酸钾晶体可以快速产生氯气,请写出该反应的化学方程式:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
.(3)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以下滴,经检查分液漏斗活塞没有堵塞,你认为应采取的措施是:
将玻璃塞上的凹槽与漏斗颈上的小孔对准(或拔去玻璃塞)
将玻璃塞上的凹槽与漏斗颈上的小孔对准(或拔去玻璃塞)
.(4)①在下列方框中画出图a中所缺装置图,并注明相关试剂的名称.

②图d装置中应放置的试剂为碱石灰,其作用是
吸收尾气中的氯气,防止空气中的水进入使S2Cl2发生水解
吸收尾气中的氯气,防止空气中的水进入使S2Cl2发生水解
.(5)某同学通过查阅资料发现:实验室常利用软锰矿(主要成分为MnO2和一些不溶性杂质)制取KMnO4晶体,其反应原理如下:3MnO2+6KOH+KClO3
| ||
①将软锰矿与固体KOH和KClO3在高温下共熔,发生反应;②
冷却,加水溶解、滤去残渣
冷却,加水溶解、滤去残渣
;③将滤液酸化,滤去MnO2沉淀;④加热浓缩、冷却结晶
加热浓缩、冷却结晶
.分析:高锰酸钾与浓盐酸反应制得氯气中含氯化氢和水蒸气,故采用洗气法除去其中杂质.氯气有毒,故实验过程中需要尾气处理.
由于S2Cl2是一种金黄色易挥发的液体,故需要冷凝装置.S2Cl2易水解,故需要干燥装置.
由于S2Cl2是一种金黄色易挥发的液体,故需要冷凝装置.S2Cl2易水解,故需要干燥装置.
解答:解:(1)冷凝蒸气一般用冷凝管,故答案为:冷凝管;
(2)高锰酸钾具有强氧化性,可把浓盐酸中的氯氧化为氯气,本身被还原成锰离子,
故答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
(3)内外空气不相通,导致烧瓶内压强大于分液漏斗内压强,液体难于流下.打开上端活塞或将玻璃塞上的凹槽与漏斗颈上的小孔对准,使内外空气相通,便于液体流下.
故答案为:将玻璃塞上的凹槽与漏斗颈上的小孔对准(或拔去玻璃塞);
(4)①先用饱和食盐水除去氯气中的氯化氢,再用浓硫酸干燥.装置图如下:
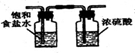
②因氯气有毒,碱石灰会与氯气反应.S2Cl2易发生水解,故碱石灰的作用还有防止空气中的水进入仪器.
故答案为:吸收尾气中的氯气,防止空气中的水进入使S2Cl2发生水解;
(5)将软锰矿与固体KOH和KClO3在高温下共熔,发生反应:
3MnO2+6KOH+KClO3
3K2MnO4+KCl+3H2O,冷却,加水溶解,过滤除去不溶性杂质和未反应的二氧化锰;滤液酸化后发生反应:3MnO42-+4H+=2MnO4-+MnO2↓+2H2O,
过滤除去二氧化锰,对滤液加热浓缩、冷却结晶,再过滤即得高锰酸钾晶体.
故答案为:冷却,加水溶解、滤去残渣;加热浓缩、冷却结晶.
(2)高锰酸钾具有强氧化性,可把浓盐酸中的氯氧化为氯气,本身被还原成锰离子,
故答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
(3)内外空气不相通,导致烧瓶内压强大于分液漏斗内压强,液体难于流下.打开上端活塞或将玻璃塞上的凹槽与漏斗颈上的小孔对准,使内外空气相通,便于液体流下.
故答案为:将玻璃塞上的凹槽与漏斗颈上的小孔对准(或拔去玻璃塞);
(4)①先用饱和食盐水除去氯气中的氯化氢,再用浓硫酸干燥.装置图如下:

②因氯气有毒,碱石灰会与氯气反应.S2Cl2易发生水解,故碱石灰的作用还有防止空气中的水进入仪器.
故答案为:吸收尾气中的氯气,防止空气中的水进入使S2Cl2发生水解;
(5)将软锰矿与固体KOH和KClO3在高温下共熔,发生反应:
3MnO2+6KOH+KClO3
| ||
过滤除去二氧化锰,对滤液加热浓缩、冷却结晶,再过滤即得高锰酸钾晶体.
故答案为:冷却,加水溶解、滤去残渣;加热浓缩、冷却结晶.
点评:制备装置要从发生装置、除杂装置、尾气处理装置和试剂性质综合考虑.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目