题目内容
一定条件下,在体积为10 L的密闭容器中,1 mol A和1 mol B进行反应:2A(g)+B(g) 2C(g),
2C(g),
经60 s达到平衡,生成0.6 mol C。下列说法正确的是
A.以A浓度变化表示的反应速率为0.001 mol·L-1·s-1
B.其他条件不变,将容器体积变为5 L,C的平衡浓度变为原来的2倍
C.其他条件不变,若增大压强,则物质A的转化率减小
D.达到平衡时,C的体积百分含量为0.353
AD
解析试题分析:A、生成0.6mol的C时,反应掉0.6mol的A,A的浓度变化量为0.06mol/L,除以时间10s得反应速率为0.001mol·L-1·s-,故A正确;B、当把容器的体积缩小时,容器内的压强增大,平衡会向气体系数和减小的方向移动,即向右移动,C的浓度大于原来的2倍,故B错误;C、增大压强,平衡向气体系数和减小的方向移动,即向右移动,A的转化率增大,故C错误;D、求出达到平衡时A、B、C三者的物质的量分别为0.4mol、0.7mol、0.6mol,C的体积百分含量为0.6除以1.7即0.353,故D正确;故选AD。
考点:化学反应速率的计算、压强对化学平衡的影响、化学平衡的计算等。

 全能闯关100分系列答案
全能闯关100分系列答案下列实验中,反应速率加快属于由催化剂引起的是
| A.氯化钠与浓硫酸混合加热后,撒入二氧化锰即放出氯气 |
| B.过氧化氢中加入几滴氯化铁溶液,可较快放出气体 |
| C.在木炭粉中加入微量氯酸钾,燃烧时极为剧烈 |
| D.用锌与稀硫酸反应制备氢气时,加入少量硫酸铜加快反应 |
溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,下列措施,不能使溶液颜色变浅的是
HBr+HBrO,下列措施,不能使溶液颜色变浅的是
| A.通入乙烯气体 | B.通入SO2气体 | C.加入NaF晶体 | D.加入NaI晶体 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( ) 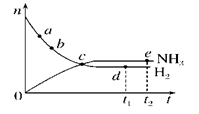
| A.c点处正反应速率和逆反应速率相等 |
| B.a点处正反应速率比b点处的大 |
| C.d点(t1时刻)和e点(t2时刻)处n(N2)不同 |
| D.t2时刻,正反应速率大于逆反应速率 |
下列叙述中一定能判断某化学平衡发生移动的是( )
| A.混合物中各组分的浓度改变 | B.正、逆反应速率改变 |
| C.混合物中各组分的含量改变 | D.混合体系的压强发生改变 |
一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A.容器Ⅰ中CO 的物质的量比容器Ⅱ中的多 |
| B.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C.容器Ⅰ、Ⅱ中正反应速率相同 |
| D.容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1 |
 2H2(g)+O2(g)。有关该反应的说法正确的是
2H2(g)+O2(g)。有关该反应的说法正确的是