题目内容
物质的量浓度相同的下列溶液中,符合按pH由小到大的顺序排列的是( )
| A、Na2CO3 NaHCO3 NaCl NH4Cl | B、Na2CO3 NaHCO3 NH4Cl NaCl | C、(NH4)2SO4 NH4Cl NaNO3 Na2S | D、NH4Cl (NH4)2SO4 Na2S NaNO3 |
分析:先是根据溶液的酸碱性将溶液分为三部分:酸性的、碱性的、中性的,再利用弱离子的水解程度:越弱越水解来比较浓度相同的溶液的pH大小即可.
解答:解:A.Na2CO3、NaHCO3均水解显碱性,碳酸钠水解程度大,碱性强,而NaCl为中性,NH4Cl水解显酸性,为pH由大到小的顺序排列,故A不选;
B.Na2CO3、NaHCO3均水解显碱性,碳酸钠水解程度大,碱性强,而NaCl为中性,NH4Cl水解显酸性,pH的排列顺序为先小后大,故B不选;
C.(NH4)2SO4、NH4Cl均水解显酸性,硫酸铵中铵根离子浓度大,水解后酸性强,pH最小,而NaNO3为中性,Na2S水解显碱性,为pH由小到大的顺序排列,故C选;
D.(NH4)2SO4、NH4Cl均水解显酸性,硫酸铵中铵根离子浓度大,水解后酸性强,pH最小,而NaNO3为中性,Na2S水解显碱性,pH由大到小再变大后减小,故D不选;
故选C.
B.Na2CO3、NaHCO3均水解显碱性,碳酸钠水解程度大,碱性强,而NaCl为中性,NH4Cl水解显酸性,pH的排列顺序为先小后大,故B不选;
C.(NH4)2SO4、NH4Cl均水解显酸性,硫酸铵中铵根离子浓度大,水解后酸性强,pH最小,而NaNO3为中性,Na2S水解显碱性,为pH由小到大的顺序排列,故C选;
D.(NH4)2SO4、NH4Cl均水解显酸性,硫酸铵中铵根离子浓度大,水解后酸性强,pH最小,而NaNO3为中性,Na2S水解显碱性,pH由大到小再变大后减小,故D不选;
故选C.
点评:本题考查了溶液pH的大小比较方法应用,把握离子水解的应用及溶液酸碱性与pH的关系为解答的关键,注意酸或是碱越弱,其阴离子水解程度越大,题目难度不大.

练习册系列答案
相关题目
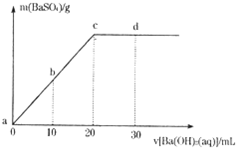 常温下,向0.1mol/L的H2SO4溶液中逐滴加入物质的量浓度相同的Ba(OH)2溶液,生成沉淀的质量和加入Ba(OH)2溶液的体积关系如下图所示,下列有关说法正确的是( )
常温下,向0.1mol/L的H2SO4溶液中逐滴加入物质的量浓度相同的Ba(OH)2溶液,生成沉淀的质量和加入Ba(OH)2溶液的体积关系如下图所示,下列有关说法正确的是( )| A、溶液的导电能力:a>b>c>d | B、溶液的pH:a<b<c<d | C、c点溶液和d点溶液均呈碱性 | D、b点溶液中c(H+)和d点溶液中c(OH-)相等 |