��Ŀ����
���¿�����Ⱦ����Ҫԭ�������ڻ�ʯȼ��ȼ�ա����Ṥҵ������β�����ŷţ���ʹ������������͵���������������С����û�ѧ��Ӧԭ���о�����������Ⱦ�ķ����ǵ�ǰ������������Ҫ�о�����֮һ��
��1����Ӧ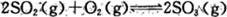 �����Ṥҵ�е���Ҫ��Ӧ�����SO2��ƽ��ת���������ڼ���β���ŷţ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ��Ϊ�����SO2��ת���ʣ����пɲ��õĴ�ʩ��
�����Ṥҵ�е���Ҫ��Ӧ�����SO2��ƽ��ת���������ڼ���β���ŷţ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ��Ϊ�����SO2��ת���ʣ����пɲ��õĴ�ʩ��
A������V2O5������ B��ͨ��������� C������ D������ѹǿ
��2��һ�������£���2L�ܱ�������ͨ��2molSO2(g)��1molO2(g)��0.2SO3(g),2min��Ӧ�ﵽƽ��ʱ,���SO2��ת����Ϊ50%����ÿ��淴Ӧ��ƽ�ⳣ��K=_________����O2��Ũ�ȱ仯��ʾ��O-2min�ڸ÷�Ӧ��ƽ������v=_________�������£������������ټ���2molSO2(g)�������´ﵽƽ��ʱSO2����ת����____________50%(�>������<������=��)
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
A��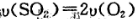 B��������ѹǿ���ֲ��䣮
B��������ѹǿ���ֲ��䣮
C��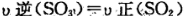 D�����������ʵ��ܶȱ��ֲ��䣮
D�����������ʵ��ܶȱ��ֲ��䣮
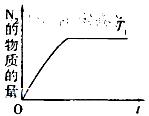
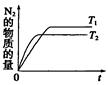
��4���ڴ�����������CH4���������ﻹԭΪN2�����������������������Ⱦ�� ��д��CH4��NO��Ӧ�Ļ�ѧ����ʽ��_________���¶�ΪT1ʱ���ܱ��������о�CH4����ԭ��������ķ�Ӧ����Ӧ�����в���N2�����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�в������¶�ΪT2(T2>T1)ʱ��n(N2)�ı仯���ߣ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ����
��1����Ӧ
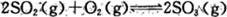 �����Ṥҵ�е���Ҫ��Ӧ�����SO2��ƽ��ת���������ڼ���β���ŷţ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ��Ϊ�����SO2��ת���ʣ����пɲ��õĴ�ʩ��
�����Ṥҵ�е���Ҫ��Ӧ�����SO2��ƽ��ת���������ڼ���β���ŷţ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ��Ϊ�����SO2��ת���ʣ����пɲ��õĴ�ʩ��A������V2O5������ B��ͨ��������� C������ D������ѹǿ
��2��һ�������£���2L�ܱ�������ͨ��2molSO2(g)��1molO2(g)��0.2SO3(g),2min��Ӧ�ﵽƽ��ʱ,���SO2��ת����Ϊ50%����ÿ��淴Ӧ��ƽ�ⳣ��K=_________����O2��Ũ�ȱ仯��ʾ��O-2min�ڸ÷�Ӧ��ƽ������v=_________�������£������������ټ���2molSO2(g)�������´ﵽƽ��ʱSO2����ת����____________50%(�>������<������=��)
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
A��
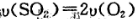 B��������ѹǿ���ֲ��䣮
B��������ѹǿ���ֲ��䣮C��
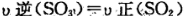 D�����������ʵ��ܶȱ��ֲ��䣮
D�����������ʵ��ܶȱ��ֲ��䣮��4���ڴ�����������CH4���������ﻹԭΪN2�����������������������Ⱦ�� ��д��CH4��NO��Ӧ�Ļ�ѧ����ʽ��_________���¶�ΪT1ʱ���ܱ��������о�CH4����ԭ��������ķ�Ӧ����Ӧ�����в���N2�����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�в������¶�ΪT2(T2>T1)ʱ��n(N2)�ı仯���ߣ���֪�÷�Ӧ�Ƿ��ȷ�Ӧ����

��1��BD ��2��5.76 0.125mol/��L��min�� �� ��3��BC
��4��CH4+4NO=2N2+CO2+2H2O
��4��CH4+4NO=2N2+CO2+2H2O

�����������1�� A������V2O5��������ֻ�ܼӿ컯ѧ��Ӧ���ʵ�ƽ�ⲻ�ƶ������������ת���ʲ��䣬����B��ͨ�����������ƽ�������ƶ������������ת����������ȷ��C���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ������������ת���ʼ�С������D���÷�Ӧ����Ϊ��������ϵ����С�ķ�Ӧ������ѹǿ��ƽ�������ƶ������������ת����������ȷ��ѡBD����2����������ʽ���м��㡣��������֪��
2SO2(g)+O2(g)
 2SO3(g)
2SO3(g)��ʼŨ�ȣ�mol/L��1 0.5 0.1
ת��Ũ�ȣ�mol/L��0.5 0.25 0.5
ƽ��Ũ�ȣ�mol/L��0.5 0.25 0.6
��ƽ��Ũ�ȴ���÷�Ӧ��ƽ�ⳣ������ʽ���㣬K=c2��SO3��/c2��SO2��c��O2��=5.76������v=��c/��t���㣬��O2��Ũ�ȱ仯��ʾ��0-2min�ڸ÷�Ӧ��ƽ������v=0.125mol/��L��min���������£������������ټ���2molSO2(g)�����������ת���ʽ��ͣ������´ﵽƽ��ʱSO2����ת����С��50%����3���жϻ�ѧƽ��״̬������Ϊ��v��=v�棬Ҫע�⡰˫��ͬʱ�����ϱ��������������жϣ�ע�⡰�������䣬�Ѵ�ƽ�⡱��A��û����ȷ�����淴Ӧ���ʣ�������Ϊ��ƽ��ı�־������B���÷�ӦΪ�������ʵ�����С�ķ�Ӧ�����ŷ�Ӧ�Ľ��У�������ѹǿ���ϱ仯��Ϊ���������䱣�ֲ���ʱ˵����Ӧ�Ѵ�ƽ�⣬��ȷ��C������v��=v�棬����Ϊƽ���־����ȷ��D�����������ʵ��ܶ�Ϊ������������Ϊƽ���־������ѡBC����4���ڴ�����������CH4���������ﻹԭΪN2�����������������������Ⱦ��CH4��NO��Ӧ���ɶ�����̼��������ˮ����ѧ����ʽΪ��CH4+4NO=2N2+CO2+2H2O���÷�ӦΪ���ȷ�Ӧ�������¶ȣ���ѧ��Ӧ���ʼӿ죬��ƽ���ʱ�����̣������¶ȣ�ƽ�������ƶ�����ƽ��ʱ���������ʵ�����С���ݴ˻���ͼ����𰸡�

��ϰ��ϵ�д�
 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
�����Ŀ
 CO2��g����H2��g����������Ӧ���ȡ�����������ͬ��2L���ݾ��ȣ������û�������������ܱ���������I�г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O,700�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ���ǣ�������
CO2��g����H2��g����������Ӧ���ȡ�����������ͬ��2L���ݾ��ȣ������û�������������ܱ���������I�г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O,700�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ���ǣ�������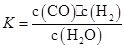 �����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬��������( )
�����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬��������( )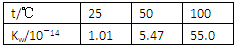
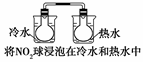

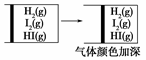

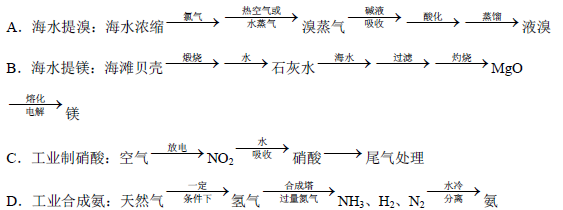
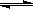 B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ���� [Cu(NH3)3]Ac��CO����֪�÷�Ӧ�Ļ�ѧƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��
[Cu(NH3)3]Ac��CO����֪�÷�Ӧ�Ļ�ѧƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��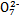 ��Cr
��Cr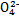 ),������Ϊ:Cr
),������Ϊ:Cr Cr2
Cr2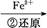 Cr3+
Cr3+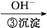 Cr(OH)3��
Cr(OH)3�� Cr2
Cr2 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq) Cr2
Cr2 3C(g)�����������У���˵����Ӧ�Ѵﵽƽ�����
3C(g)�����������У���˵����Ӧ�Ѵﵽƽ�����