题目内容
下列叙述中正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件下和点燃条件下的 AH不同 AH不同 |
| B.常温下,反应2A(s)+B(g)=2C(g)+D(g)不能自发进行,则该反应的焓变一定大于零 |
| C.需要加热的化学反应,生成物的总能量一定高于反应物的总能量 |
| D.化学反应中必伴随着能量的变化,其表现形式只有热能 |
B
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件下和点燃条件下的
 H相同,反应热取决于生成物和反应物总能量的相对大小。
H相同,反应热取决于生成物和反应物总能量的相对大小。C.反应吸放热和反应条件无关,吸热反应和放热反应都可能需要加热才能进行。反应的吸放热取决于反应物和生成物的总能量的相对大小;
D.化学反应中必伴随着能量的变化,其表现形式可以为热能、电能、光能等很多形式。
点评:考查反应中的能量变化,及反应热的相关知识点。

练习册系列答案
相关题目
 成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中)
成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中) CH3OH(g) ΔH1
CH3OH(g) ΔH1 (g) ΔH =-1275.6 kJ·mol-1
(g) ΔH =-1275.6 kJ·mol-1
 ,则H2SO4和Ba(OH)2反应的中和热为:
,则H2SO4和Ba(OH)2反应的中和热为:
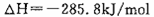
 。
。
 移向 (填“a”或“b”)电极,
移向 (填“a”或“b”)电极, (3)乙池中发生反应的离子方程式为 ;
(3)乙池中发生反应的离子方程式为 ;
 (标准状况下)。如何检验A处的产物 。
(标准状况下)。如何检验A处的产物 。 熔点、沸点数据如下:
熔点、沸点数据如下:
 62
62 750
750 。
。 试剂中最适宜的试剂是
试剂中最适宜的试剂是