题目内容
3.用石墨作电极电解3mol•L-1KCl和0.5mol•L-1Al2(SO4)3的1L混合溶液时,如图电解变化曲线合理的是( )| A. | 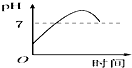 | B. | 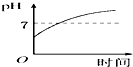 | C. |  | D. | 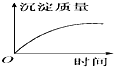 |
分析 Al2(SO4)3水解呈酸性,离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,阳极依次发生:2Cl--2e-═Cl2↑,4OH--4e-═O2↑+2H2O;阴极发生2H++2e-=H2↑,结合相关离子的物质的量解答该题.
解答 解:混合溶液的体积为1L,
则n(Cl-)=3mol,n(Al3+)=1mol,
离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,
阳极发生:2Cl--2e-═Cl2↑,Cl-离子全部放电,失去3mol电子,
阴极反应为2H++2e-═H2↑,得到3mol电子,生成3molOH-,
而1molAl3+与3molOH-发生Al3++3OH-═Al(OH)3↓,
剩余溶液为K2SO4,溶液呈中性,pH=7,
继续电解,为电解水,溶液pH不变,沉淀不溶解.
故选:D.
点评 本题考查电解原理,为高考常见题型,侧重于学生分析能力和计算能力的考查,注意把握离子的放电顺序,难度中等.

练习册系列答案
相关题目
13.(1)如图1,在试管Ⅰ和Ⅱ中分别加入3mL稀盐酸(均足量),再将装有0.3g NaHCO3和0.3g Na2CO3粉末的小气球分别套在Ⅰ和Ⅱ的管口.将气球内的NaHCO3和Na2CO3同时倒入试管中,请回答下列问题:

①试管Ⅰ和试管Ⅱ中发生反应的离子方程式分别为HCO3-+H+═CO2↑+H2O、CO32-+2H+═CO2↑+H2O.
②加入固体后,试管Ⅰ(填“Ⅰ”或“Ⅱ”)上的气球膨胀较快.
(2)为了研究Na2CO3、NaHCO3与盐酸的反应过程中的热效应,该同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
请你帮助填写相关内容:
①该研究报告的题目是碳酸钠、碳酸氢钠与盐酸反应过程中热效应的探究.
②通过上述实验可得出:
Na2CO3溶液和盐酸的反应是放热(填“吸热”或“放热”,下同)反应,对应的图象
为B(见图2)NaHCO3溶液和盐酸的反应是吸热反应,对应的图象为A.

①试管Ⅰ和试管Ⅱ中发生反应的离子方程式分别为HCO3-+H+═CO2↑+H2O、CO32-+2H+═CO2↑+H2O.
②加入固体后,试管Ⅰ(填“Ⅰ”或“Ⅱ”)上的气球膨胀较快.
(2)为了研究Na2CO3、NaHCO3与盐酸的反应过程中的热效应,该同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后的最高温度 |
| ① | 50mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 50mL水 | 3.2g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 50mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ④ | 50mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
①该研究报告的题目是碳酸钠、碳酸氢钠与盐酸反应过程中热效应的探究.
②通过上述实验可得出:
Na2CO3溶液和盐酸的反应是放热(填“吸热”或“放热”,下同)反应,对应的图象
为B(见图2)NaHCO3溶液和盐酸的反应是吸热反应,对应的图象为A.
14.下列有关叙述中不正确的是( )
| A. | 相同温度下,0.02 mol•L-1的醋酸溶液与0.01 mol•L-1的醋酸溶液中的c(H+)之比小于2:1 | |
| B. | 相同温度下,0.1 mol•L-1 (NH4)2SO4溶液与0.1 mol•L-1NH4NO3溶液中c(NH4+)之比大于2:1 | |
| C. | 在0.1 mol•L-1NaOH溶液中逐滴加入0.1 mol•L-1CH3COOH溶液,当溶液pH=7时,加入CH3COOH溶液的体积与NaOH溶液的体积比小于2:1 | |
| D. | 40℃时,pH=7的(NH4)2SO4与NH3•H2O的混合溶液中c(NH4+)与c(SO42-)之比小于2:1 |
11. 原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )
原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )
 原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )
原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )| A. | 两分子原硅酸脱去一分子水得到的H6Si2O7分子中有6个Si-O键 | |
| B. | 两个硅氧四面体,彼此用一个角氧相连后,形成的Si2O76-离子中各键角均为109°28′ | |
| C. | 3个硅氧四面体彼此用3个角氧相连后,形成的Si3O96-离子呈链状 | |
| D. | n个硅氧四面体彼此用四个角氧连接后的晶体是二氧化硅 |
8. 汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.
汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.
2NO(g)+2CO(g)═2CO2(g)+N2(g)△H1=-746.5kJ•mol-1
已知:2C(s)+O2(g)═2CO(G)△H2=-221kJ•mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
则N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表:
①c1合理的数值为D(填字母) A.4.20 B.4.00 C.3.50 D.2.50
②前2s内的平均反应速率 v(CO2 )=3.75×10-4 mol/(L.s)
③不能作为判断该反应达到平衡状态的标志是ab.(填字母标号)
a.2v正(CO)=v疗(N2)
b.容器中混合气体的密度保持不变
c.容器中气体的压强不变
d.CO2的体积分数不变
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如图所示:
则曲线I、Ⅱ、Ⅲ对应的实验编号依次为③②①
(4)已知:CO通入新制的银氨溶液可生成银镜,同时释放一种能使湿润的红色石蕊试纸变蓝的气体.某温度下,向1L密闭容器中充入1molNO和1molCO,反应达到平衡后,将平衡混合气通入足量新制的银氨溶液中.生成43.2g Ag,则该温度下,反应:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g)的化学平衡常数K=160
(5)CO可作燃料电池的烯气.用Li2CO3和Na2CO3的熔融盐混合物做电解质,空气与CO2的混合气为正极助燃气,制得650℃下工作的燃料电池.该电池总反应为2CO+O2═2CO2,则负极反应式为2CO+2CO32--4e-═4CO2.
 汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.
汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.2NO(g)+2CO(g)═2CO2(g)+N2(g)△H1=-746.5kJ•mol-1
已知:2C(s)+O2(g)═2CO(G)△H2=-221kJ•mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
则N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表:
| 时间/s | 0 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol•L-1 | 10.0 | c1 | 1.50 | 1.00 | 1.00 |
| c(CO)10-3mol•L-1 | 3.60 | c2 | 2.75 | 2.70 | 2.70 |
②前2s内的平均反应速率 v(CO2 )=3.75×10-4 mol/(L.s)
③不能作为判断该反应达到平衡状态的标志是ab.(填字母标号)
a.2v正(CO)=v疗(N2)
b.容器中混合气体的密度保持不变
c.容器中气体的压强不变
d.CO2的体积分数不变
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如图所示:
| 实验 序号 | T/℃ | NO初始浓 度/10-3mol•L-1 | CO初始浓 度/10-3mol•L-1 | 催化剂的比表面积/㎡•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
(4)已知:CO通入新制的银氨溶液可生成银镜,同时释放一种能使湿润的红色石蕊试纸变蓝的气体.某温度下,向1L密闭容器中充入1molNO和1molCO,反应达到平衡后,将平衡混合气通入足量新制的银氨溶液中.生成43.2g Ag,则该温度下,反应:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g)的化学平衡常数K=160
(5)CO可作燃料电池的烯气.用Li2CO3和Na2CO3的熔融盐混合物做电解质,空气与CO2的混合气为正极助燃气,制得650℃下工作的燃料电池.该电池总反应为2CO+O2═2CO2,则负极反应式为2CO+2CO32--4e-═4CO2.
15.一种新型燃料电池,用两根金属Pt作电极插入KOH溶液中,然后向两极分别通入甲烷和氧气,其电极反应式为:X极:CH4+10OH--8e-=CO32-+7H2O;
Y极:4H2O+2O2+8e-=8OH-.
下列关于此燃料电池的说法中,错误的是( )
Y极:4H2O+2O2+8e-=8OH-.
下列关于此燃料电池的说法中,错误的是( )
| A. | X为负极,Y为正极 | |
| B. | 该电池工作时,X极附近溶液的碱性增强 | |
| C. | 在标准状况下,通入5.6LO2完全反应后,有1mol电子发生转移 | |
| D. | 工作一段时间后,KOH的物质的量减少 |
12.下列实验方案合理的是( )
| A. | 鉴别集气瓶中的甲烷和乙烯:移去玻璃片,分别点燃,观察火焰的颜色及是否有黑烟 | |
| B. | 检验酒精中的少量水:向酒精中加入足量生石灰 | |
| C. | 制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 | |
| D. |  证明溴乙烷与NaOH醇溶液共热生成乙烯:用如右图所示的实验装置 |
 .
. .
.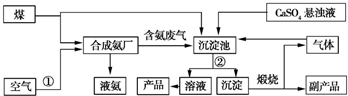
 2NH3.
2NH3. CaCO3↓+(NH4)2SO4.
CaCO3↓+(NH4)2SO4.