题目内容
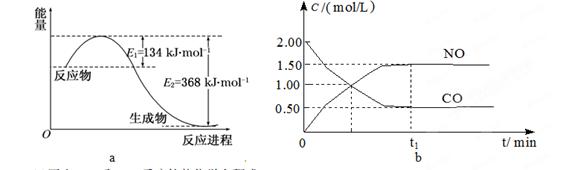
某反应过程能量变化如图所示,下列说法正确的是


| A.反应过程a有催化剂参与 |
| B.该反应为放热反应,热效应等于ΔH |
| C.改变催化剂,可改变该反应的活化能 |
| D.有催化剂条件下,反应的活化能等于E1+E2 |
B C
试题分析:A.由图示可知反应过程a需要的活化能较高,没有催化剂参与。错误。B.由于反应物的能量高于生成物的能量,多余的能量就以热能的形式释放出来。所以该反应为放热反应,热效应等于反应物与生成物能量的差值ΔH。正确。C.改变催化剂,改变了反应途径,降低了反应的活化能,但是反应热不变。正确。D.无论是否存在催化剂,反应的活化能等于反应物与生成物的能量的差值,等于ΔH。错误。

练习册系列答案
相关题目

 2H2↑+O2↑
2H2↑+O2↑ 2NH3(g)(放热反应)。下列描述中正确的是
2NH3(g)(放热反应)。下列描述中正确的是 CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。
CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。
 还原为N2,一段时间后,溶液的碱性
还原为N2,一段时间后,溶液的碱性

 FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K; O2(g)===H2O(g) ΔH1=a kJ·mol-1;
O2(g)===H2O(g) ΔH1=a kJ·mol-1; 2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ