题目内容
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A.常温常压下,1.5g甲基(-CH3)中含有的电子数为NA
B.加热条件下,含0.2molH2SO4的浓硫酸与足量铜反应,转移电子数小于0.2NA
C.常温下,1LpH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9NA
D.0.lmol环氧乙烷(![]() )中含有的共价键数为0.3NA
)中含有的共价键数为0.3NA
【答案】B
【解析】
A.常温常压下,一个-CH3中含有9个电子,1.5g甲基(-CH3)为![]() =0.1mol,含有的电子数为0.9NA,故A错误;
=0.1mol,含有的电子数为0.9NA,故A错误;
B.Cu只能和浓硫酸反应,和稀硫酸不反应,0.2mol的浓硫酸不能反应完全,则生成SO2的分子数小于0.1NA,转移电子数小于0.2NA,故B正确;
C.常温下,1LpH=9的CH3COONa溶液中c(H+)=10-9mol/L,水电离的氢氧根离子浓度为c(OH-)=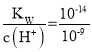 =10-5mol/L,根据H2OH++OH-,则发生电离的水分子数为1L×10-5 mol/L×NA=1×10-5NA,故C错误;
=10-5mol/L,根据H2OH++OH-,则发生电离的水分子数为1L×10-5 mol/L×NA=1×10-5NA,故C错误;
D.一个环氧乙烷分子中中含7个共价键,则0.1mol环氧乙烷中含有的共价键数为0.1mol ×7×NA =0.7NA,故D错误;
答案选B。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】用中和滴定法测定某烧碱的纯度,试根据实验回答:
(1)称取4.1g烧碱样品。将样品配成250mL待测液,需要的主要玻璃仪器除烧杯、玻璃棒外还需__________________ 、______________________。
(2)取10.00mL待测液,用___________________量取。
(3)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,以酚酞为指示剂,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶,直到看到_________即可判断达到滴定终点。
(4)根据下列数据,计算待测烧碱溶液的浓度为:___________(结果保留四位有效数字)。(假设烧碱中不含有与酸反应的杂质)
滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)滴定过程,下列情况会使测定结果偏高的是____________________(填序号)。
①酸式滴定管用水洗后便装液体进行滴定;
②碱式滴定管水洗后,就用来量取待测液;
③锥形瓶用蒸馏水洗涤后,又用待测液润洗;
④滴定过快成细流、将碱液溅到锥形瓶壁而又未摇匀洗下;
⑤盐酸在滴定时溅出锥形瓶外;
⑥滴加盐酸,溶液颜色褪去但不足半分钟又恢复红色;
⑦滴定前,酸式滴定管有气泡,滴定后消失;
⑧记录起始体积时,仰视读数,终点时俯视。
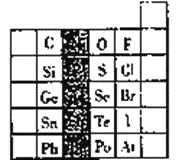
【题目】下表是周期表中的一部分,根据A-I在周期表中的位置,请按要求回答下列问题:
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | A | |||||||
二 | D | E | G | I | ||||
三 | B | C | F | H |
(1)A-I中元素,化学性质最不活泼的是______(用元素符号),还原性最强的单质是______(用元素符号);
(2)A-I中最高价氧化物的水化物酸性最强的酸是______(用化学式);
(3)用电子式表示D元素最高价氧化物的形成过程_______________________________ ;
D元素最高价氧化物的结构式为______
(4)写出B与C两元素最高价氧化物的水化物之间反应的离子方程式___________________ .
【题目】乙酰苯胺(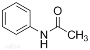 )在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过苯胺(
)在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过苯胺(![]() )和乙酸酐(
)和乙酸酐(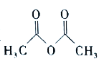 )反应制得。已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的溶解度如下。
)反应制得。已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的溶解度如下。
温度/℃ | 20 | 25 | 50 | 80 | 100 |
溶解度/(g/100g水) | 0.46 | 0.56 | 0.84 | 3.45 | 5.5 |
实验室制备乙酰苯胺的步骤如下(部分装置省略):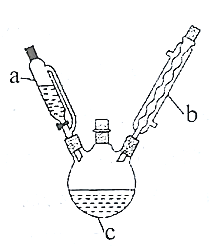
Ⅰ.粗乙酰苯胺的制备。将7mL(0.075mol)过量乙酸酐放入三颈烧瓶c中,在a中放入5mL(0.055mol)新制得的苯胺。将苯胺在室温下逐滴滴加到三颈烧瓶中。苯胺滴加完毕,在石棉网上用小火加热回流30min,使之充分反应。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有100mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用__洗涤晶体2-3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯。将上述制得的粗乙酰苯胺固体移入250mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,__、洗涤、干燥后称量产品为5.40g。
回答下列问题:
(1)仪器b的名称是__。
(2)步骤I中,减压过滤的优点是过滤速度快,同时所得固体更干燥,用滤液而不用蒸馏水冲洗烧杯的原因是__;洗涤晶体最好选用__(填字母)。
A.乙醇 B.CCl4 C.冷水 D.乙醚
(3)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是__。
(4)步骤Ⅱ中,洗涤干燥前的操作是___。上述提纯乙酰苯胺的方法叫__。
(5)乙酰苯胺的产率为___。(计算结果保留3位有效数字)
【题目】用图所示装置检验乙烯时不需要除杂的是
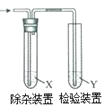
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |