题目内容
【题目】乙酰苯胺(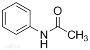 )在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过苯胺(
)在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过苯胺(![]() )和乙酸酐(
)和乙酸酐(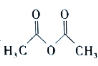 )反应制得。已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的溶解度如下。
)反应制得。已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的溶解度如下。
温度/℃ | 20 | 25 | 50 | 80 | 100 |
溶解度/(g/100g水) | 0.46 | 0.56 | 0.84 | 3.45 | 5.5 |
实验室制备乙酰苯胺的步骤如下(部分装置省略):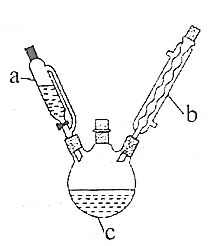
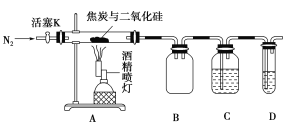
Ⅰ.粗乙酰苯胺的制备。将7mL(0.075mol)过量乙酸酐放入三颈烧瓶c中,在a中放入5mL(0.055mol)新制得的苯胺。将苯胺在室温下逐滴滴加到三颈烧瓶中。苯胺滴加完毕,在石棉网上用小火加热回流30min,使之充分反应。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有100mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用__洗涤晶体2-3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯。将上述制得的粗乙酰苯胺固体移入250mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,__、洗涤、干燥后称量产品为5.40g。
回答下列问题:
(1)仪器b的名称是__。
(2)步骤I中,减压过滤的优点是过滤速度快,同时所得固体更干燥,用滤液而不用蒸馏水冲洗烧杯的原因是__;洗涤晶体最好选用__(填字母)。
A.乙醇 B.CCl4 C.冷水 D.乙醚
(3)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是__。
(4)步骤Ⅱ中,洗涤干燥前的操作是___。上述提纯乙酰苯胺的方法叫__。
(5)乙酰苯胺的产率为___。(计算结果保留3位有效数字)
【答案】球形冷凝管 用滤液冲洗烧杯可减少乙酰苯胺的溶解损失 C 减少趁热过滤时乙酰苯胺的损失 过滤 重结晶 72.7%
【解析】
根据图示,装置c中制备乙酰苯胺,乙酸酐与新制的苯胺在加热条件下发生取代反应生成乙酰苯胺和乙酸;减压过滤的速度快,水分抽取的更充分;用蒸馏水冲洗烧杯会使结晶的乙酰苯胺晶体溶解,产率降低;步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的主要是避免溶剂的损失、温度的降低可能导致产物析出,影响产率;上述提纯乙酰苯胺的过程中,步聚I和步骤Ⅱ两次对制得的产品进行结晶处理;根据题中数据和分析反应物的用量,根据不足量计算出生成乙酰苯胺的物质的量,再根据实际上生成的乙酰苯胺的质量计算出产率,据此分析解答。
(1) 根据图示,仪器b的名称是球形冷凝管;
(2) 用蒸馏水冲洗烧杯会使结晶的乙酰苯胺晶体溶解,产率降低,则用滤液而不用蒸馏水冲洗烧杯的原因是用滤液冲洗烧杯可减少乙酰苯胺的溶解损失;乙酰苯胺易溶于有机溶剂,根据不同温度下乙酰苯胺在水中的溶解度表数据可知,温度越高,溶解度越大,则洗涤晶体最好选用冷水,答案选C;
(3)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水可以避免在趁热过滤时因溶剂的损失或温度的降低导致乙酰苯胺的损失,影响产率,所以补加少量蒸馏水的目的是减少趁热过滤时乙酰苯胺的损失;
(4) 步骤Ⅱ中,洗涤干燥前要将晶体分离出来,所以操作是过滤;上述提纯乙酰苯胺的过程中,步聚I和步骤Ⅱ两次对制得的产品进行结晶处理,提纯乙酰苯胺的方法叫重结晶;
(5) 7mL(0.075mol)乙酸酐和5mL(0.055mol)新制得的苯胺反应制取乙酰苯胺,反应为![]() +
+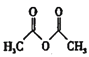 →
→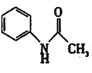 +CH3COOH,根据反应可知,乙酸酐过量,理论上反应生成的乙酰苯胺的物质的量为0.055mol,则该实验苯乙酰胺的产率=
+CH3COOH,根据反应可知,乙酸酐过量,理论上反应生成的乙酰苯胺的物质的量为0.055mol,则该实验苯乙酰胺的产率=![]() =72.7%。
=72.7%。

【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
【题目】查阅资料:元素铬(Cr)在溶液中主要以Cr3+(蓝紫色) 、Cr(OH)4-(绿色) 、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
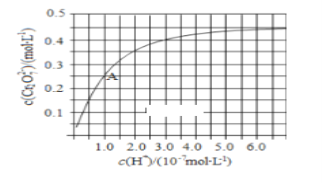
(1)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如右图所示。
①用离子方程式表示Na2CrO4溶液中的转化反应____________。
②由图可知,溶液酸性增大,CrO42的平衡转化率________(填“增大“减小”或“不变”)。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH____0(填“>”“<”或“=”)。
(2)欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去.已知:某含铬废水处理的主要流程如图所示:
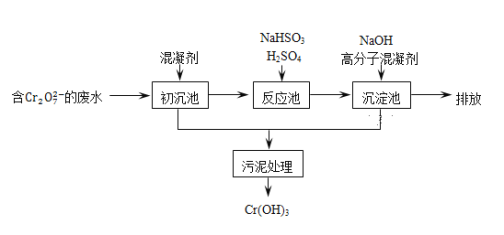
①初沉池中加入的混凝剂是K2SO4·Al2(SO4)3·24H2O,其作用为__________(用离子方程式表示).
②反应池中用NaHSO3将酸性废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为________.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子的先后顺序是____________。
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.2 |
Cr3+ | 6.0 | 8.0 |
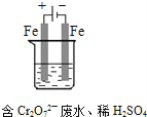
(3)工业可用电解法来处理含 Cr2O72-废水。实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑,Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是__________,得到的金属阳离子在阴极区可沉淀完全,用电解法处理该溶液中0.01mol Cr2O72-时,至少得到沉淀的质量是__________ g。