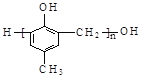题目内容
【题目】在下图所示装置中加入一定量的铁粉,分液漏斗中加入一定体积浓度为12 mol·L-1的硝酸,加热打开分液漏斗的活塞,使其充分反应后,
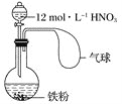
下列微粒:①![]() 、② Fe3+、③H+、④ NO、⑤ NO2,在该装置中一定大量存在的( )
、② Fe3+、③H+、④ NO、⑤ NO2,在该装置中一定大量存在的( )
A.①B.①⑤C.②④⑤D.①②③⑤
【答案】B
【解析】
12 mol·L-1的HNO3为浓硝酸,反应生成的为NO2,从下边几个角度
(1)铁过量,则反应方程式为:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O,2Fe(NO3)3+Fe=3Fe(NO3)2,最后剩余的离子是Fe2+和![]() ;
;
(2)硝酸过量,则反应方程式为Fe+6 HNO3=Fe(NO3)3+3NO2↑+3H2O,最后剩余的离子是Fe3+、H+和![]() ;
;
(3)铁与硝酸都消耗完,则反应方程式为:Fe +6 HNO3=Fe(NO3)3+3NO2↑+3H2O,2Fe(NO3)3+Fe=3 Fe(NO3)2,铁被消耗完,而Fe(NO3)3有剩余,最后剩余的离子为Fe2+、Fe3+、![]() 。
。
根据题目分析的三种情况,可以得出:一定大量存在的是①![]() 和⑤NO2,故答案B正确。
和⑤NO2,故答案B正确。

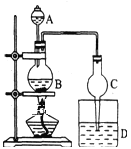
【题目】如图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。


(1)该实验反应的反应方程式为:___。
(2)仪器a的名称是___。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃__(填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用上图中___(填“甲”“乙”或“丙”)装置。
②称取5.6g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.896L,则铁粉的转化率为__。(转化率=![]() )
)
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:
步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
Ⅰ.取样,滴加KSCN溶液 | 溶液不变红色(Fe3+与KSCN溶液反应显红色) | ①Fe3O4+8H+=Fe2++2Fe3++4H2O ②____ | Ⅲ.反应后的溶液中阳离子为___ |
Ⅱ.取样,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现白色沉淀,迅速变为灰绿色,最终变为红褐色 | ①___ ②Fe2++2OH—=Fe(OH)2↓(白色) 4Fe(OH)2+2H2O+O2=4Fe(OH)3 |