��Ŀ����
����Ŀ��������֪ij��Ӧ�з�Ӧ����������У�KMnO4��H2SO4��MnSO4��H2C2O4��K2SO4��H2O��һ��δ֪��X��
(1)��֪0.5 molH2C2O4�ڷ�Ӧ��ʧȥ1 mol��������X����X�Ļ�ѧʽΪ______________��
(2)���������ͻ�ԭ������ƽ��ϵ���������з����У����õ����ű������ת�Ƶķ������Ŀ��
___________________________
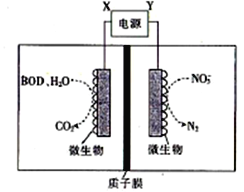
������ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+���ӹ�ҵ��ˮ�л������������ͽ���ͭ�Ĺ���������ͼ��ʾ��
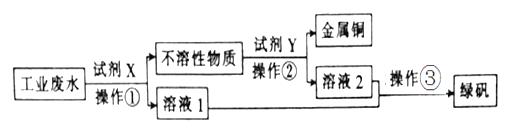
(1)ͼ�в�����Ϊ______________��������Ϊ_______________________________��
(2)�Լ�XΪ______���ѧʽ�����������漰�����ӷ�Ӧ����ʽΪ___________________��
���𰸡�CO2 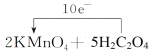 ���� ����Ũ������ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2��
���� ����Ũ������ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2��
��������
����1����֪0.5mol H2C2O4�ڷ�Ӧ��ʧȥ1mol��������X��̼Ԫ�ػ��ϼ�Ϊx��KMnO4����ԭΪMnSO4����ϵ����غ�������̼Ԫ�ػ��ϼۣ�2��[x-��+3��]��0.5mol=1��x=+4�������ɵ�XΪCO2��
��2�����������ǿ�����ԣ�����ѡ�����������������H2C2O4��C�Ļ��ϼ�Ϊ+3�ۣ�CO2��C�Ļ��ϼ�Ϊ+4�ۣ�Ҫѡ��ʧ���ӵ���������ԭ��������ѡ��H2C2O4����ԭ�����ɸ����������������������μӷ�Ӧ�����ݷ�Ӧǰ��Ԫ���غ㣬ˮ���������У�
�÷�Ӧ�л��ϼ۵ı仯Ϊ��KMnO4��MnSO4��MnԪ����+7����+2�ۣ�һ��KMnO4���ӵ�5�����ӣ�H2C2O4��CO2��CԪ����+3����+4�ۣ�һ��H2C2O4ʧȥ2�����ӣ����Ե�ʧ���ӵ���С������Ϊ10������KMnO4�ļ�����Ϊ2��H2C2O4�ļ�����Ϊ5������Ԫ�ظ���ԭ���غ���ƽ���ʷ�ӦΪ��2KMnO4+5H2C2O4+3H2SO4=2MnSO4+10CO2��+8H2O+K2SO4���õ����ű������ת�Ƶķ������ĿΪ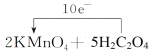 ��
��
��ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+����������ͼ�п���֪������ɻ�������������ͭ���ȼӹ������۰�ͭ�û����������Լ�XΪ���ۣ�����1�ǹ��ˣ����������������û�����ͭ���й����������������ᣬ���˼��õ�����ͭ����Һ2ΪFeSO4������Һ1�ϲ�����Ũ������ȴ�ᾧ�õ��̷���
(1)ͼ�в�����Ϊ���ˣ�������Ϊ����Ũ������ȴ�ᾧ��
(2)�Լ�XΪFe���������漰�����ӷ�Ӧ����ʽΪFe + 2H+ = Fe2+ + H2����