题目内容
【题目】氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有关数据见下表:
化学式 | Cl2O | ClO2 | Cl2O7 |
相对分子质量 | 87 | 67.5 | 183 |
沸点/℃ | 2 | 9.7 | 81 |
完成下列填空:
(1)Cl2O是酸的酸酐,Cl2O电子式为 .
(2)下列能判断Cl和O两种元素非金属性强弱的是(选填编号).
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2 , 其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2﹣)和氯酸盐,其离子方程式是 , 氧化产物 . (填离子符号)
(5)一定条件下,在水溶液中1mol Cl﹣、ClO ![]() (x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示).
(x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示). 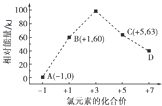
【答案】
(1)HClO;![]()
(2)ac
(3)Cl2O7、Cl2O、ClO2结构不相似,不符合分子间作用力对沸点影响的变化规律
(4)2ClO2+2OH﹣=ClO2﹣+ClO3﹣+H2O;ClO3﹣
(5)ClO4﹣;3ClO﹣(aq)=ClO3﹣(aq)+2Cl﹣(aq)△H=﹣117kJ/mol
【解析】解:(1)酸酐与对应酸中Cl元素的化合价相同,则Cl2O是为HClO的酸酐,Cl2O的结构为Cl﹣O﹣Cl,其电子式为 ![]() ,所以答案是:HClO;
,所以答案是:HClO; ![]() ;(2)a.氧化氯的分子式中O为负价,则非金属性O大于Cl,故正确; b.与金属反应得电子的数目,不能比较非金属性,故错误;c.气态氢化物的稳定性强的为水,则非金属性O大于Cl,故正确d.O元素不存在最高价氧化物对应水化物,故错误;所以答案是:ac;(3)上表中相对分子质量是Cl2O7>Cl2O>ClO2 , 其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是Cl2O7、Cl2O、ClO2结构不相似,不符合分子间作用力对沸点影响的变化规律,所以答案是:Cl2O7、Cl2O、ClO2结构不相似,不符合分子间作用力对沸点影响的变化规律;(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2﹣)和氯酸盐,为氧化还原反应,离子反应为2ClO2+2OH﹣=ClO2﹣+ClO3﹣+H2O,Cl元素失去电子被氧化,则氧化产物为ClO3﹣ , 所以答案是:2ClO2+2OH﹣=ClO2﹣+ClO3﹣+H2O;ClO3﹣;(5)由图可知,D中Cl元素的化合价为+7价,则D为ClO4﹣;B→A+C结合转移电子守恒得该反应方程式为3ClO﹣=ClO3﹣+2Cl﹣ , △H=(63kJ/mol+2×0kJ/mol)﹣3×60kJ/mol=﹣117kJ/mol,所以该热化学反应方程式为3ClO﹣(aq)=ClO3﹣(aq)+2Cl﹣(aq)△H=﹣117kJ/mol,所以答案是:ClO4﹣;3ClO﹣(aq)=ClO3﹣(aq)+2Cl﹣(aq)△H=﹣117kJ/mol.
;(2)a.氧化氯的分子式中O为负价,则非金属性O大于Cl,故正确; b.与金属反应得电子的数目,不能比较非金属性,故错误;c.气态氢化物的稳定性强的为水,则非金属性O大于Cl,故正确d.O元素不存在最高价氧化物对应水化物,故错误;所以答案是:ac;(3)上表中相对分子质量是Cl2O7>Cl2O>ClO2 , 其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是Cl2O7、Cl2O、ClO2结构不相似,不符合分子间作用力对沸点影响的变化规律,所以答案是:Cl2O7、Cl2O、ClO2结构不相似,不符合分子间作用力对沸点影响的变化规律;(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2﹣)和氯酸盐,为氧化还原反应,离子反应为2ClO2+2OH﹣=ClO2﹣+ClO3﹣+H2O,Cl元素失去电子被氧化,则氧化产物为ClO3﹣ , 所以答案是:2ClO2+2OH﹣=ClO2﹣+ClO3﹣+H2O;ClO3﹣;(5)由图可知,D中Cl元素的化合价为+7价,则D为ClO4﹣;B→A+C结合转移电子守恒得该反应方程式为3ClO﹣=ClO3﹣+2Cl﹣ , △H=(63kJ/mol+2×0kJ/mol)﹣3×60kJ/mol=﹣117kJ/mol,所以该热化学反应方程式为3ClO﹣(aq)=ClO3﹣(aq)+2Cl﹣(aq)△H=﹣117kJ/mol,所以答案是:ClO4﹣;3ClO﹣(aq)=ClO3﹣(aq)+2Cl﹣(aq)△H=﹣117kJ/mol.