题目内容
【题目】室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )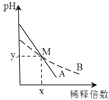
A.稀释前,c(A)>10 c(B)
B.中和等浓度等体积的盐酸时,B用的体积较多
C.M点时A和B的浓度相等
D.在M点,A,B两种碱溶液中阳离子的物质的量浓度相等
【答案】D
【解析】解:A.AB稀释相同倍数,A的pH变化大,则A的碱性强,稀释前,设c(A)=0.1mol/L,c(B)>0.01mol/L,则c(A)<10c(B),故A错误;
B.稀释前A溶液中氢氧根离子浓度大于B溶液中,即A的浓度大于B,所以中和等浓度等体积的盐酸时,A用的体积较多,故B错误;
C.M点AB溶液pH相同,A的碱性强,A的电离度大于B,所以浓度B大于A的浓度,不相等,故C错误;
D.M点AB溶液pH相同,氢氧根离子浓度相同,由电荷守恒c(A+)+c(H+)=c(OH﹣),c(B+)+c(H+)=c(OH﹣)可知c(A+)=c(B+),所以M点A、B两种碱溶液中阳离子的物质的量浓度相等,故D正确;
故选D.
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.

【题目】氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有关数据见下表:
化学式 | Cl2O | ClO2 | Cl2O7 |
相对分子质量 | 87 | 67.5 | 183 |
沸点/℃ | 2 | 9.7 | 81 |
完成下列填空:
(1)Cl2O是酸的酸酐,Cl2O电子式为 .
(2)下列能判断Cl和O两种元素非金属性强弱的是(选填编号).
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2 , 其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2﹣)和氯酸盐,其离子方程式是 , 氧化产物 . (填离子符号)
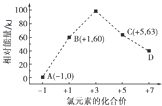
(5)一定条件下,在水溶液中1mol Cl﹣、ClO ![]() (x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示).
(x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示).