题目内容
11.化学实验要符合“绿色化学”理念.某实验小组对“铜与浓硝酸反应”进行了探究性实验.试回答下列问题: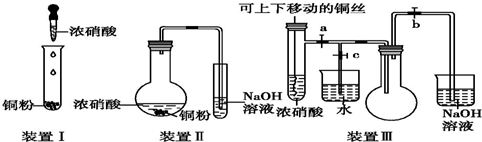
(1)写出铜和浓硝酸反应的化学方程式:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
(2)与装置Ⅰ相比,装置Ⅱ的优点是无氮的氧化物逸出,避免了对空气的污染,装置Ⅲ除具有装置Ⅱ的优点外,还具有的优点是可控制反应随时进行,随时停止.
(3)在装置Ⅲ中,若使NO2气体充满烧瓶,应先关闭弹簧夹c,再打开弹簧夹a、b;
当气体充满烧瓶后,将铜丝提起,然后把a、b、c都关闭,并把烧瓶置于冰水中,下列情况不变的是BD.
[已知:二氧化氮气体在温度降低时,有利于部分转化为无色的四氧化二氮(N2O4)气体;
2NO2?N2O4]
A.颜色 B.质量 C.气体的平均相对分子质量 D.密度 E.压强
(4)为了验证NO2与水的反应,欲使烧杯中的水进入烧瓶的操作是关闭a和c,打开b,对烧瓶进行水浴加热,待气体不再放出时关闭b,停止加热,打开c.
分析 (1)铜和浓硝酸反应生成硝酸铜、二氧化氮和水;
(2)对生成的氮氧化物吸收防止污染空气,装置Ⅲ无污染,随时进行和停止;
(3)在装置Ⅲ中,若使NO2气体充满烧瓶应关闭c,打开ab,过量二氧化氮可以被氢氧化钠溶液吸收;
根据此步骤是为了NO2气体充满②试管;根据存在反应2NO2?N2O4是化学平衡,结合平衡移动原理分析;
(4)验证NO2与水的反应,欲使烧杯中的水进入烧瓶,需要让二氧化氮与水接触发生反应.
解答 解:(1)因铜和浓硝酸反应生成硝酸铜、二氧化氮和水,Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
(2)乙装置能吸收NO2气体,所以无氮的氧化物逸出,可避免环境污染;C装置能控制反应,可使反应随时进行,随时停止,
故答案为:无氮的氧化物逸出,可避免环境污染;可使反应随时进行,随时停止;
(3)为了NO2气体充满②试管,应先关闭c,然后打开a、b,
在25度时试管中的二氧化氮会转化为四氧化二氮,2NO2(g)?N2O4(g)(正反应为放热反应),若把试管置于100度的沸水中.
A.由于该反应是放热反应,置于100℃的沸水中,平衡会逆向移动,NO2增多,那么颜色会变深,故A错误;
B.根据质量守恒定律知,二氧化氮转化前后,物质的总质量不变,故B正确;
C.二氧化氮转化前后,气体的总质量不变,物质的量改变,所以平均摩尔质量改变,故C错误;
D.根据质量守恒定律知,二氧化氮转化前后,物质的总质量不变,试管的容积不变,所以气体的密度始终不变,故D正确;
E.二氧化氮转化前后,气体的物质的量改变,所以压强改变,故E错误;
,故选BD;
故答案:c;ab;BD.
(4)为了让二氧化氮与水接触发生反,关闭a和c,打开b,对烧瓶进行水浴加热,待气体不再放出时关闭b,停止加热,打开c,
故答案为:关闭a和c,打开b,对烧瓶进行水浴加热,待气体不再放出时关闭b,停止加热,打开c.
点评 本题考查了氮氧化合物的性质等知识点,难度中等,易错题是(3)题,容易忽略二氧化氮和四氧化二氮之间的转化,温度对该反应的影响,错误的认为二氧化氮和沸水反应生成硝酸和一氧化氮,导致选择错误.

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案①SO2 ②Fe3+ ③Fe2+ ④HCl ⑤H2O2.
| A. | ①②③ | B. | ①③ | C. | ①③⑤ | D. | ①③④⑤ |
Ⅰ.甲、乙两支试管分别盛甲烷和氯气的混合气体(以体积比1:1混合),其中一支用黑纸包好,将它们置于光线一般的室内,等待片刻,观察现象.请填写下表:
| 实验现象 | 实验结论 | |
| 甲 | 在光照条件下,试管内气体颜色变浅了;试管内壁上出现了油状液滴. | CH4与Cl2在光照条件下 发生化学反应 |
| 乙 | 迅速剥开黑纸,立即观察,试管内气体颜色为黄绿色. | CH4与Cl2在无光照条件下不发生化学反应. |
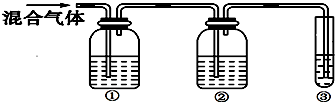
Ⅱ.为探究乙烯与溴的加成反应,因实验室制得的乙烯中通常会含有少量的SO2等杂质气体,该同学认为应先除去杂质,再通入溴水中.为此,他设计了如图所示的实验装置:
请回答:
(1)①、②、③装置中可盛放的试剂是:①A、②B、③C.(填序号)
A.NaOH溶液 B.品红 C.溴水 D.酸性高锰酸钾溶液
(2)除杂后,观察到溴水褪色,结合所学内容得出结论:乙烯可与溴水发生加成反应.请写出化学反应方程式CH2=CH2+Br2→
 .
.Ⅲ.为了探究苯与溴反应生成溴苯的实验,该同学采用下图所示装置,请分析装置并完成下列题目:

(1)关闭F夹,打开C夹,向装有少量苯的三颈烧瓶中由A口加入过量溴,再加入少量铁屑,塞住A口,则三颈烧瓶中发生反应的化学方程式为
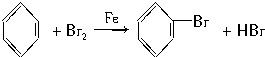
(2)D、E试管内出现的现象为石蕊溶液变红、出现淡黄色沉淀.
通过探究,该同学得出结论:甲烷、乙烯和苯在不同的条件下均能与卤素反应.
Ⅳ.现有H2、Cl2、乙烷、乙烯这四种原料,请你设计一种制取一氯乙烷的最佳实验方案,请用方程式表示出来(注意:原料不一定要全部选用).H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl、CH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl.
| A. | 混合气体的体积恒定不变 | |
| B. | 混合气体的颜色不再改变 | |
| C. | 混合气体的平均摩尔质量不变 | |
| D. | I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
| A. | 铝在空气中能很快形成氧化膜 | |
| B. | 铝箔失去金属光泽,氧化铝包裹着金属铝 | |
| C. | 氧化铝的熔点比铝高 | |
| D. | 氧化铝与盐酸不反应 |

 .
. .
.