题目内容
16.可逆反应H2(g)+I2(g)?2HI(g) 达到平衡状态时的标志是( )| A. | 混合气体的体积恒定不变 | |
| B. | 混合气体的颜色不再改变 | |
| C. | 混合气体的平均摩尔质量不变 | |
| D. | I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、两边气体计量数相等,所以混合气体的体积一直不变,故A错误;
B、混合气体的颜色不再改变,说明碘蒸气的浓度保持不变,达平衡状态,故B正确;
C、从反应发生,混合气体的平均摩尔质量一直不变,故C错误;
D、当体系达平衡状态时,I2在混合气体中的体积分数与H2在混合气体中的体积分数可能相等,也可能不等,与各物质的初始浓度及转化率有关,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
14.某有机物的结构简式如图所示,有关该有机物的叙述正确的是( )


| A. | 分子中含有3 种官能团 | |
| B. | 在一定条件下,能发生取代、氧化、酯化和加聚反应 | |
| C. | 该物质分子中最多可以有10 个碳原子在同一平面上 | |
| D. | 1 mol 该物质最多可与5 mol H2发生加成反应 |
1.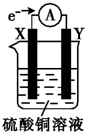 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )| A. | 外电路中电流方向为X→Y | |
| B. | 若电极材料分别为锌片和铜片,则Y为锌片 | |
| C. | X极上发生还原反应 | |
| D. | 若电极材料都是金属,则金属活动性:X>Y |
8.分子组成为C4H9OH并能发生催化氧化反应但不能得到醛的有机化合物有( )
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
6.在(NH4)2Fe(SO4)2溶液中逐滴加入100mL 1mol/L的Ba(OH)2溶液,把所得沉淀过滤、洗涤、干燥,得到的固体质量不可能是( )
| A. | 35.3g | B. | 33.5g | C. | 32.3g | D. | 11.3g |
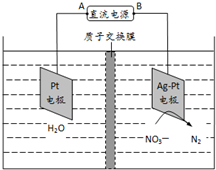 化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.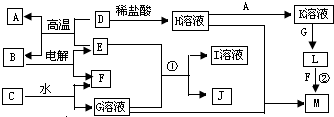
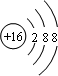
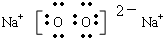 ,C物质中所含化学键类型离子键、非极性共价键.
,C物质中所含化学键类型离子键、非极性共价键.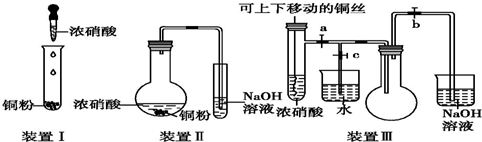
 .
.