题目内容
10.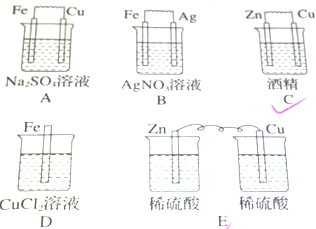
上述装置中能形成原电池的是AB,该原电池工作时,负极发生氧化,电极反应式为Fe-2e-=Fe2+;正极发生还原,电极反应式为O2+4e-+2H2O=4OH-、2Ag++2e-=2Ag.
分析 根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应判断;负极失电子发生氧化反应,正极得电子发生还原反应,据此分析判断.
解答 解:A、不能自发的发生氧化还原反应,不能形成原电池,故A错误;
B、铁为负极,Ag为正极,可形成原电池,故B正确;
C、酒精不导电,不能形成原电池,故C错误;
D、没有活泼性不同的2个电极,不能形成原电池,故D错误;
E、没有形成闭合回路,不能形成原电池,故E错误.
AB中负极失电子发生氧化反应,反应式为Fe-2e-=Fe2+,正极得电子发生还原反应,反应式为O2+4e-+2H2O=4OH-、2Ag++2e-=2Ag,
故答案为:B;氧化;Fe-2e-=Fe2+;还原;O2+4e-+2H2O=4OH-、2Ag++2e-=2Ag.
点评 本题考查原电池的组成及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法,难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
3.以下化学用语正确的是( )
| A. | 乙醇的分子式CH3CH2OH | B. | CH3COCH3的官能团名称:醚键 | ||
| C. | 苯的最简式:CH | D. | 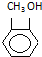 的类别:醇类 的类别:醇类 |
15.央视3•15晚会曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,β4用作一些燃料的替代品,其结构式为 .下列有关二甲醚的叙述正确的是( )
.下列有关二甲醚的叙述正确的是( )
 .下列有关二甲醚的叙述正确的是( )
.下列有关二甲醚的叙述正确的是( )| A. | 二甲醚是一种有机物,属于非电解质 | |
| B. | 4.6g该物质中含有共价键的数目为2×6.02×1022 | |
| C. | 二甲醚和乙醇互为同分异构体且和甲醇互为同系物 | |
| D. | 标准状况下,燃烧11.2L二甲醚一定生成22.4LCO2 |
 氨气的制取及性质探究(图中夹持装置均已略去).
氨气的制取及性质探究(图中夹持装置均已略去).
 、SiO
、SiO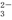 、CO
、CO 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验: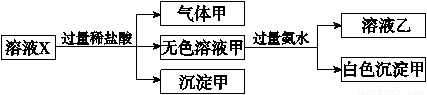
 和SiO
和SiO