题目内容
10.现有常温下的四份溶液:①0.01mol/L 醋酸溶液;②0.01mol/L盐酸;③pH=12的氨水;④pH=12的NaOH溶液.下列说法正确的是( )| A. | ①中水的电离程度最小,③中水的电离程度最大 | |
| B. | 将②、③混合,若有pH=7,则消耗溶液的体积:②<③ | |
| C. | 将①、④混合,若有c(CH3COO-)>c(H+),则c(OH-)>c(Na+) | |
| D. | 将四份溶液分别稀释100倍后,溶液的pH:③>④,①>② |
分析 A、酸碱对水的电离起到抑制作用,酸中的氢离子或碱中的氢氧根离子浓度越大,抑制程度越大;
B、氨水是弱碱,等体积混合时溶液呈碱性,所以盐酸体积大于氨水溶液的体积;
C、将①、④混合体积不同混合后溶液不一定成碱性,中性溶液中也存在c(CH3COO-)>c(H+);
D、稀释相同倍数,弱电解质存在电离平衡;
解答 解:A.酸或碱能抑制水的电离,当溶液中氢离子或氢氧根离子浓度越大,水的电离程度越小,pH=12的氨水和pH=12的NaOH溶液中c(OH-)=0.01moL/L,0.01moL/L HCl中c(H+)=0.01moL/L,所以这三种溶液中水的电离程度相同,0.01mol/L CH3COOH中(H+)<0.01moL/L,所以醋酸中水的电离程度最大,故A错误;
B、②③若等体积混合后溶液呈碱性,若有pH=7,则消耗溶液的体积:②>③,故B错误;
C、若将①、④等体积混合,醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,有c(CH3COO-)>c(H+),若混合后溶液呈中性时存在C(Na+)=c(CH3COO-)>C(OH-)=c(H+),故C错误;
D、将四份溶液稀释相同倍数后溶液的pH:氨水存在电离平衡,溶液中氢氧根离子浓度大于氢氧化钠溶液中氢氧根离子,pH值③>④,同浓度醋酸和盐酸稀释相同倍数,醋酸存在电离平衡,醋酸溶液中氢离子浓度小于盐酸溶液中的氢离子浓度,酸性越弱,pH越大,所以溶液PH②<①,故D正确;
故选D.
点评 本题考查了弱电解质的电离平衡应用,主要是对水的电离影响,溶液酸碱性的判断,溶液稀释的PH变化,关键是酸碱反应后溶液酸碱性的判断,题目难度中等.

练习册系列答案
相关题目
1.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

关于该固体混合物,下列说法正确的是( )

关于该固体混合物,下列说法正确的是( )
| A. | 一定含有Al,其质量为4.5g | |
| B. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定不含FeCl2,可能含有MgCl2和AlCl3 |
1.工业上,可用CO和H2合成CH3OH,此反应的化学方程式为CO(g)+2H2(g)?CH3OH(g).该反应不同温度下的平衡常数如表所示:
下列叙述中正确的是( )
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
| A. | 该反应的正反应是吸热反应 | |
| B. | 100℃时,向体积为V1L的恒容密闭容器中充入2mol CO和4mol H2,达到平衡时,CO的转化率为40%,则V1=12 | |
| C. | 250℃时,向体积为V2L的恒容密闭容器中充入3mol CO和3mol H2,达到平衡时,混合气体中CO的体积分数为50% | |
| D. | 250℃时,向体积为V2L的恒容密闭容器中充入3mol CO和3mol H2,达到平衡时,混合气体中CH3OH(g)的体积分数为62.5% |
5.在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )

| A. | 该反应的化学方程式为5A+4B?4C | |
| B. | 2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4 | |
| C. | 用B的浓度变化表示0-2min时间内的速率为2mol/(L•min) | |
| D. | 2min前,正反应速率逐渐减小,逆反应速率逐渐增大,但是正反应速率大于逆反应速率 |
15.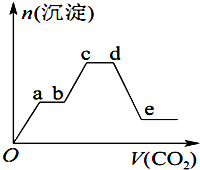 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述错误的是( )
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述错误的是( )
 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述错误的是( )
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述错误的是( )| A. | Oa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O | |
| B. | bc段与cd段所消耗CO2的体积相同 | |
| C. | bc段反应的离子方程式是2AlO${\;}_{2}^{-}$+3H2O+CO2═2Al(OH)3↓+CO${\;}_{3}^{2-}$ | |
| D. | de段沉淀减少是由于BaCO3固体的消失 |
2.在100mL 0.1mol•L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度也增大,可采用的方法是( )
| A. | 升高一定的温度 | |
| B. | 加入100 mL 0.1 mol•L-1的醋酸溶液 | |
| C. | 加入少量的0.5 mol•L-1的硫酸 | |
| D. | 加入少量的1 mol•L-1的NaOH溶液 |
19.把11.7g NaCl固体放人500ml的烧杯中,加入150ml蒸馏水搅拌至完全溶解,然后将溶液全部转移到容器M中,再用蒸馏水稀释至完全充满;从中取出溶液100ml,该溶液恰好与50mL 0.40mol•L-lAgN03溶液完全反应.则M的体积为( )
| A. | 100 ml. | B. | 250 ml. | C. | 500 ml. | D. | 1 L. |
20.CH3-CH2-${\;}_{\;}^{16}$OH、CH3-CH2-${\;}_{\;}^{18}$OH分别与CH3COOH反应,生成的酯的相对分子质量大小关系( )
| A. | 前者大于后者 | B. | 前者小于后者 | C. | 前者等于后者 | D. | 无法确定 |
