题目内容
16.混合下列各组物质使之充分反应,加热蒸干产物并高温下灼烧至质量不变,最终残留固体为纯净物的是( )| A. | 向CuSO4溶液中加入适量铁粉 | |
| B. | 在Na2SiO3溶液中通入过量CO2气体 | |
| C. | 等物质的量的NaHCO3与Na2O2溶于水 | |
| D. | 等物质的量浓度、等体积的FeCl3与KI溶液混合 |
分析 A.反应生成硫酸亚铁和Cu,高温下灼烧至质量不变得到铜和硫酸铁;
B.向Na2SiO3的溶液中通入过量的二氧化碳,生成硅酸沉淀,高温下灼烧至质量不变得到二氧化硅;
C.等物质的量的NaHCO3与Na2O2固体混合,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,过氧化钠再与二氧化碳、水反应;
D.等物质的量浓度、等体积的FeCl3与KI溶液混合,2FeCl3+2KI=2FeCl2+KCl+I2.
解答 解:A.向CuSO4溶液中加入适量铁粉,一定生成硫酸亚铁,反应生成硫酸亚铁和Cu,高温下灼烧至质量不变得到铜和硫酸铁,无论Fe是否过量,产物均为混合物,故A不选;
B.向Na2SiO3的溶液中通入过量的二氧化碳,生成硅酸沉淀,高温下灼烧至质量不变得到二氧化硅,为纯净物,故B选;
C.等物质的量的NaHCO3与Na2O2固体混合,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,过氧化钠再与二氧化碳、水反应,蒸干灼烧后的固体为碳酸钠和NaOH,为混合物,故C不选;
D.等物质的量浓度、等体积的FeCl3与KI溶液混合,2FeCl3+2KI=2FeCl2+KCl+I2,加热蒸干产物并高温下灼烧至质量不变为氧化铁和氯化钾,得到为混合物,故D不选.
故选B.
点评 本题综合考查物质的性质、发生的化学反应以及分离等操作,侧重于学生的分析能力、实验能力和基础知识的综合运用,为高考常见题型,题目难度中等,选项C为解答的难点.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
7.能够用键的强度解释的是( )
| A. | N2的化学性质比O2稳定 | B. | HNO3易挥发,H2SO4难挥发 | ||
| C. | 常温、常压下,溴呈液态,碘呈固态 | D. | 稀有气体很难发生化学反应 |
4.把①蔗糖,②淀粉,③纤维素,④乙酸乙酯在稀硫酸存在下分别进行水解,最终产物只有1种的是( )
| A. | ①和② | B. | 只有③ | C. | 只有④ | D. | 只有②和③ |
1.I.如图1为向25mL 0.1mol/L NaOH溶液中逐滴滴加0.2mol/LCH3COOH溶液过程中溶液pH的变化曲线.请回答:
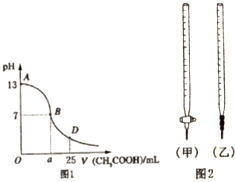
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?否(选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?AB区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项A(选填字母).
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是D.
A.c(OH-)大于c(CH3COO-)B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)=2c(Na+)(填“>”“<”或“=”).
II.t℃时,某稀硫酸溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=13:
(5)该温度下水的离子积常数KW的数值为10-13.
(6)该温度下(t℃),将100mL 0.1mol/L的稀H2SO4与100mL 0.4mol/L的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=12.

(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?否(选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?AB区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项A(选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (甲) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 石蕊 | (乙) |
| D | 酸 | 碱 | 石蕊 | (乙) |
A.c(OH-)大于c(CH3COO-)B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)=2c(Na+)(填“>”“<”或“=”).
II.t℃时,某稀硫酸溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=13:
(5)该温度下水的离子积常数KW的数值为10-13.
(6)该温度下(t℃),将100mL 0.1mol/L的稀H2SO4与100mL 0.4mol/L的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=12.
5.下列化合物命名正确的是( )
| A. | CH2=CH-CH=CH21,4-丁二烯 | B. |  3-丁醇 3-丁醇 | ||
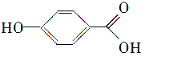
| C. |  甲基苯酚 甲基苯酚 | D. |  2-甲基丁烷 2-甲基丁烷 |
8.下列化学用语正确的是( )
| A. | 乙烯的结构简式CH2CH2 | B. | Na2O2中氧元素的化合价为-2 | ||
| C. | Cl-的结构示意图: | D. | 乙酸的最简式:CH2O |
 .
. .
. .
.