题目内容
11.结合如图中所示转化关系回答有关问题.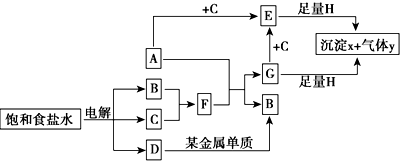
(1)液态F能否导电否(填“能”或“否”).
(2)A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%.A发生腐蚀的主要原因是(填写下面的选项序号)b.
a.直接与氧气发生化学腐蚀
b.通过原电池反应发生腐蚀
c.因溶于水而消耗掉(①、②只答其一)
①若你选定选项a或c,请写出相应的化学方程式:无;
②若你选定选项b,请写出负极的电极反应式Fe-2e-═Fe2+.
(3)气体y的密度约是空气密度的1.1倍,则沉淀x的化学式是Fe(OH)3.气体y的结构式O=O
(4)写出D+某金属单质→B的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(5)将(4)反应设计成原电池,请画出原电池的装置图(标出正、负极、溶液).
分析 电解饱和食盐水得到NaOH、H2、Cl2,B、C、D分别为NaOH、H2、Cl2中的一种,B与C反应得到F,F与金属A反应得到B与G,D与某种金属反应得到B,应金属Al与碱的反应,可推知B为H2、C为Cl2、D为NaOH,F为HCl.由A与C(氯气)的反应及G与C(氯气)反应可知,金属A为变价金属,且A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%,可推知A是Fe,则G为FeCl2,E为FeCl3,E、G均匀足量的H反应得到沉淀x与气体y,气体y的密度约是空气密度的1.1倍,则y相对分子质量为29×1.1=32,可推知H为Na2O2、x为Fe(OH)3,气体y为O2,据此解答.
解答 解:电解饱和食盐水得到NaOH、H2、Cl2,B、C、D分别为NaOH、H2、Cl2中的一种,B与C反应得到F,F与金属A反应得到B与G,D与某种金属反应得到B,应金属Al与碱的反应,可推知B为H2、C为Cl2、D为NaOH,F为HCl.由A与C(氯气)的反应及G与C(氯气)反应可知,金属A为变价金属,且A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%,可推知A是Fe,则G为FeCl2,E为FeCl3,E、G均匀足量的H反应得到沉淀x与气体y,气体y的密度约是空气密度的1.1倍,则y相对分子质量为29×1.1=32,可推知H为Na2O2、x为Fe(OH)3,气体y为O2.
(1)HCl为共价化合物,液态情况下不导电,故答案为:否;
(2)生铁中含有铁和碳,铁、碳和电解质溶液能构成原电池,铁作负极而加速被腐蚀,故选b;
负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,
故答案为:b;Fe-2e-═Fe2+;
(3)由上述分析可知,x为Fe(OH)3,y为O2,结构式为O=O,
故答案为:Fe(OH)3;O=O;
(4)D+某金属单质→B的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(5)将(4)反应设计成原电池的装置图为: ,
,
故答案为: .
.
点评 本题考查无机物的推断,推断突破口为A及饱和食盐水电解产物、转化中特殊反应,需要学生熟练掌握元素化合物知识,难度中等.

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
| A. | 由红外光谱可知,该有机物中至少有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子 | |
| C. | 仅由核磁共振氢谱无法得知其分子中的氢原子总数 | |
| D. | 若 A的化学式为C3H8O,则其结构简式可能为 |
| A. | CH3-CH=CH2和CH2=CH2的最简式相同 | |
| B. | 乙二醇和丙三醇为同系物 | |
| C. | CH≡CH和C6H6含碳量相同 | |
| D. | 2-甲基-2-丙醇不能被催化氧化成相应的醛 |
| A. | 同温同压下,相同体积的物质,所含的粒子数必相等 | |
| B. | 任何条件下,等质量的乙烯和一氧化碳所含的分子数必相等 | |
| C. | 1 L一氧化碳气体的质量一定比1 L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数目一定相等 |

| A. | Si | B. | Na+ | C. | Al | D. | SO2 |
| A. | 向CuSO4溶液中加入适量铁粉 | |
| B. | 在Na2SiO3溶液中通入过量CO2气体 | |
| C. | 等物质的量的NaHCO3与Na2O2溶于水 | |
| D. | 等物质的量浓度、等体积的FeCl3与KI溶液混合 |
| A. | QCl2 | B. | RCl | C. | SCl3 | D. | TCl |
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2④1s222s2p63s23p4 原子半径最大的是① | |
| B. | 具有下列价电子排布式的原子中,①3s23p1②3s23p2③3s23p3④3s23p4第一电离能最大是③ | |
| C. | ①Na、K、Rb ②N、P、Si ③Na、P、Cl,元素的电负性随原子序数增大而递增的是③ | |
| D. | 某主族元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+ |
 某同学想研究氨基酸的分离和鉴定的方法,已知实验室中有0.5%的赖氨酸、脯氨酸、缬氨酸、苯丙氨酸、亮氨酸溶液以及它们的混合液(各组份浓度均为0.5% );现提供如下器材和试剂:
某同学想研究氨基酸的分离和鉴定的方法,已知实验室中有0.5%的赖氨酸、脯氨酸、缬氨酸、苯丙氨酸、亮氨酸溶液以及它们的混合液(各组份浓度均为0.5% );现提供如下器材和试剂: