题目内容
下列说法正确的是( )
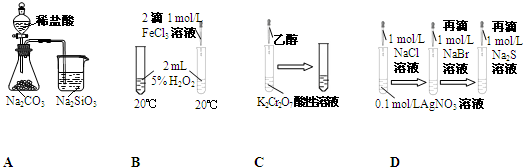
| A、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 | ||
| B、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水.②0.1mol/L盐酸.③0.1mol/L氯化镁溶液.④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ | ||
C、已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=
| ||
| D、I2在乙醇中溶解度很大,但从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
考点:pH的简单计算,弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.醋酸为弱电解质,醋酸稀释过程中电离程度增大,溶液中氢离子的物质的量增大,稀释10倍后溶液的pH<4;
B.氯化银饱和溶液中存在沉淀溶解平衡,饱和溶液中的溶度积是常数,只随温度变化;依据溶度积是常数分别依据离子浓度越小沉淀溶解平衡的程度分析判断;
C.弱电解质的电离平衡常数只与温度有关,温度不变,电离平衡常数不变;
D.乙醇能够与水以任意比混溶,所以不能用无水乙醇代替四氯化碳萃取碘水中的碘单质.
B.氯化银饱和溶液中存在沉淀溶解平衡,饱和溶液中的溶度积是常数,只随温度变化;依据溶度积是常数分别依据离子浓度越小沉淀溶解平衡的程度分析判断;
C.弱电解质的电离平衡常数只与温度有关,温度不变,电离平衡常数不变;
D.乙醇能够与水以任意比混溶,所以不能用无水乙醇代替四氯化碳萃取碘水中的碘单质.
解答:
解:A.醋酸属于弱酸,浓度越大,电离程度越小,所以常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液中氢离子的数目增大,溶液的3<pH<4,故A错误;
B.通过溶度积是一定温度下的常数,分别得到:①蒸馏水中含银离子浓度和氯离子浓度相同;②0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L;抑制溶解沉淀平衡;③0.1mol?L-1MgCl2溶液中Cl-浓度为0.2mol/l,抑制沉淀溶解平衡;④0.1mol/L硝酸银溶液中Ag+浓度为0.1mol/L,Cl-浓度越大,Ag+浓度越小,则Ag+离子浓度大小为:④>①>②>③,故B错误;
C.弱电解质的电离平衡常数只与温度有关,温度不变是,醋酸的电离平衡常数不会发生变化,但稀释醋酸溶液时促进醋酸电离,导致醋酸的电离度增大,即α增大,故C错误;
D.萃取操作时,萃取剂不能与原溶剂相溶,由于乙醇与水相互溶解,所以从碘水中提取单质碘时,不能用无水乙醇代替CCl4,故D正确;
故选D.
B.通过溶度积是一定温度下的常数,分别得到:①蒸馏水中含银离子浓度和氯离子浓度相同;②0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L;抑制溶解沉淀平衡;③0.1mol?L-1MgCl2溶液中Cl-浓度为0.2mol/l,抑制沉淀溶解平衡;④0.1mol/L硝酸银溶液中Ag+浓度为0.1mol/L,Cl-浓度越大,Ag+浓度越小,则Ag+离子浓度大小为:④>①>②>③,故B错误;
C.弱电解质的电离平衡常数只与温度有关,温度不变是,醋酸的电离平衡常数不会发生变化,但稀释醋酸溶液时促进醋酸电离,导致醋酸的电离度增大,即α增大,故C错误;
D.萃取操作时,萃取剂不能与原溶剂相溶,由于乙醇与水相互溶解,所以从碘水中提取单质碘时,不能用无水乙醇代替CCl4,故D正确;
故选D.
点评:本题考查了弱电解质的电离、影响弱电解质电离的因素等知识点,明确弱电解质电离特点是解本题关键,注意电离平衡常数、水解平衡常数、化学平衡常数、溶度积常数等都只与温度有关,与溶液的酸碱性无关,为易错点.

练习册系列答案
相关题目
下图所示的实验装置或操作合理的是( )
A、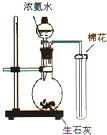 制氨气 |
B、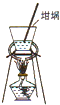 蒸发、结晶 |
C、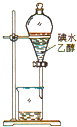 萃取碘 |
D、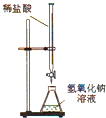 酸碱中和滴定 |
下列有关说法不正确的是( )
| A、互为同系物的有机物其组成元素相同,且结构必须相似 |
| B、分子组成相差一个或若干个CH2原子团的化合物一定互为同系物 |
| C、分子式为C3H6与C6H12的两种有机物一定互为同系物 |
| D、互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数) |
下列离子方程式正确的是( )
| A、氧化铁溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O | ||||
| B、在AgCl沉淀中加入碘化钾溶液:AgCl(s)+I-(aq)═AgI (s)+Cl-(aq) | ||||
C、铜与浓硫酸共热:Cu+4H++SO42-
| ||||
D、电解氯化镁溶液:2Cl-+2H2O
|
下列说法正确的是( )
| A、H、D、T表示三种氢原子 |
| B、原子最外层少于4个电子的元素均是金属元素 |
| C、稀有气体元素最外层电子数均为8个 |
| D、目前人们已发现了5000多种核素,说明发现了5000多种元素 |
下列分离提纯方法不正确的是( )
| A、分离碘和氯化钠,用升华法 |
| B、分离硝酸钾和氯化钠固体,先加水溶解再用过滤法 |
| C、除去酒精中少量的水,先加生石灰再用蒸馏法 |
| D、分离苯和酸性高锰酸钾溶液,用分液法 |
下列表示对应化学反应的离子方程式正确的是( )
A、NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-
| ||||
| B、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | ||||
| C、将少量醋酸溶液滴加到Na2CO3溶液中的反应:CH3COOH+CO32-=CH3COO-+HCO3- | ||||
| D、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |