题目内容
下列实验现象及其对应的结论正确的是( )
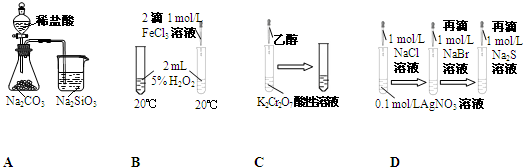

| 实验 | 现象 | 结论 |
| A | 锥形瓶中有气体产生,烧杯中液体变浑浊 | Cl、C、Si非金属性依次减弱 |
| B | 右边试管中冒出的气泡快 | FeCl3能加快H2O2分解速率 |
| C | 试管中橙色溶液变为绿色 | 乙醇发生消去反应生成乙烯 |
| D | 试管中溶液依次出现白色、淡黄色、黑色沉淀 | 溶解度:AgCl<AgBr<Ag2S |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.制取的二氧化碳中含有HCl,HCl干扰二氧化碳的反应;
B.催化剂能加快反应速率;
C.重铬酸钾具有强氧化性,能氧化乙醇;
D.发生沉淀的转化,向更难溶的方向移动.
B.催化剂能加快反应速率;
C.重铬酸钾具有强氧化性,能氧化乙醇;
D.发生沉淀的转化,向更难溶的方向移动.
解答:
解:A.盐酸易挥发,与碳酸钠、硅酸钠均发生化学反应,制取的二氧化碳中含有HCl,图中装置不能说明二氧化碳与硅酸钠溶液反应,则不能比较碳酸与硅酸的酸性,故A错误;
B.右边试管中冒出的气泡快,说明氯化铁作催化剂,加快双氧水分解,故B正确;
C.重铬酸钾具有强氧化性,能氧化乙醇,自身被还原,所以溶液颜色发生变化,故C错误;
D.发生沉淀的转化,向更难溶的方向移动,则由白色固体先变为淡黄色,后变为黑色,可知溶解性:AgCl>AgBr>Ag2S,故D错误;
故选B.
B.右边试管中冒出的气泡快,说明氯化铁作催化剂,加快双氧水分解,故B正确;
C.重铬酸钾具有强氧化性,能氧化乙醇,自身被还原,所以溶液颜色发生变化,故C错误;
D.发生沉淀的转化,向更难溶的方向移动,则由白色固体先变为淡黄色,后变为黑色,可知溶解性:AgCl>AgBr>Ag2S,故D错误;
故选B.
点评:本题考查了实验方案评价,涉及沉淀的转化、氧化还原反应、催化剂等知识点,明确实验原理是解本题关键,易错选项是A,要排除HCl的干扰.

练习册系列答案
相关题目
选取萃取剂将碘水中的碘萃取出来,下列物质不能作为萃取剂是( )
| A、CCl4 |
| B、酒精 |
| C、直馏汽油 |
| D、苯 |
把0.1mol铝投入100mL 3mol/L的NaOH溶液中充分反应,再滴入120mL 1mol/L的H2SO4溶液,其结果是
( )
( )
| A、溶液的pH>7 |
| B、得到澄清透明的溶液 |
| C、得到浑浊液体 |
| D、先有沉淀生成后逐渐溶解 |
下列说法正确的是( )
| A、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 | ||
| B、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水.②0.1mol/L盐酸.③0.1mol/L氯化镁溶液.④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ | ||
C、已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=
| ||
| D、I2在乙醇中溶解度很大,但从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
化学源于生活,同时又服务于生活,下列说法不合理的是( )
| A、田间焚烧秸秆污染环境,浪费资源 |
| B、泄露在海洋中的大量原油能被海洋生物迅速分解,不会导致生态灾难,不需要治理 |
| C、推广使用无磷洗涤剂,可有效减少水体的富营养化 |
| D、服用铬含量超标的药用胶囊会对从体健康造成危害 |
在指定的环境中,下列离子一定能大量共存的为( )
| A、由H2O电离出的C(H+)=10-13的溶液中:Na+,S2-,SO42-,NH4+ |
| B、与Al反应放出氢气的溶液中:Fe3+,Cl-,Ca2+,NO3- |
| C、使甲基橙变红的溶液中:NH4+,S2-,K+,SO32- |
| D、室温下,PH=1的溶液:Na+,Fe3+,SO42-,NO3- |
向澄清饱和石灰水中放入一小块钠,不可能出现的现象是( )
| A、钠熔化成光亮银白色的小球 |
| B、浮在液面快速游动 |
| C、液体底部出现银白色固体 |
| D、液面有水雾 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
| B、标准状况下,2.24L NO2中含分子数有0.1NA个 |
| C、常温常压下,44g CO2中含有22NA个电子 |
| D、1mol?L-1 NaCl溶液含阴阳离子总数有2NA个 |
对于苯乙烯(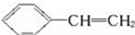 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
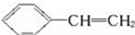 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )| A、①②③⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、①②③④⑤⑥ |