题目内容
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是 ( )

A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
D. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
【答案】C
【解析】
A项,图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快,A项错误;
B项,图乙表明,其他条件相同时,NaOH溶液的浓度越大,溶液的碱性越强,pH越大,H2O2分解速率越快,B项错误;
C项,图丙表明,其他条件相同有一定浓度的Mn2+存在时,H2O2的分解速率:0.1mol/LNaOH溶液>1.0mol/LNaOH溶液>0mol/LNaOH,但不是“溶液碱性越强,H2O2分解速率越快”,碱性溶液中Mn2+对H2O2的分解速率有影响,图丁表明,其他条件相同时,Mn2+浓度越大,H2O2分解速率越快,根据上述分析,图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大,C项正确;
D项,图丙表明,其他条件相同时,H2O2的分解速率:0.1mol/LNaOH溶液>1.0mol/LNaOH溶液>0mol/LNaOH,少量Mn2+存在时,并不是“溶液碱性越强,H2O2分解速率越快”,D项错误;
答案选C。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】2016年度国家科学技术奖授予我国诺贝尔奖获得者屠呦呦,表彰她在抗疟疾青蒿素方面的研究。
(查阅资料)青蒿素熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水几乎不溶。
I.实验室用乙醚提取青蒿素的工艺流程如下:

(1)在操作I前要对青蒿进行粉碎,其目的是________________
(2)操作II的名称是_____________。
(3)操作III进行的是重结晶,其操作步骤为_____ 、_____、______、过滤、洗涤、干燥
II.已知青蒿素是一种烃的含氧衍生物为确定它的化学式,进行了如下实验:

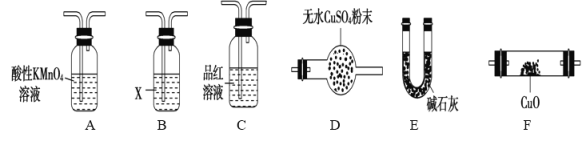
实验步骤:①连接装置,检查装置的气密性。②称量E、F中仪器及药品的质量。③取14.10g青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量。
(4)装置E、F应分别装入的药品为_______________、___________________。
(5)实验测得:
装置 | 实验前 | 实验后 |
E | 24.00g | 33.90g |
F | 100.00g | 133.00g |
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为______。
(6)若使用上述方法会产生较大实验误差,你的改进方法是________________________。