题目内容
【题目】HCl和NaOH(待测)中和滴定时计算公式c(NaOH)=______。H2SO4和NaOH(待测)中和滴定时计算公式c(NaOH)=____。
【答案】

【解析】
根据盐酸、硫酸与氢氧化钠反应的物质的量关系,结合物质的量浓度定义式计算、书写。
HCl和NaOH发生中和反应的方程式为:HCl+NaOH=NaCl+H2O,当二者恰好反应时,n(NaOH)=n(HCl),由于在溶液中c=![]() ,所以滴定时待测NaOH溶液浓度计算公式为:c(NaOH)=
,所以滴定时待测NaOH溶液浓度计算公式为:c(NaOH)=  ;H2SO4和NaOH发生中和反应的方程式为:H2SO4+2NaOH=Na2SO4+2H2O,当二者恰好反应时,n(NaOH)=2n(H2SO4),由于在溶液中c=
;H2SO4和NaOH发生中和反应的方程式为:H2SO4+2NaOH=Na2SO4+2H2O,当二者恰好反应时,n(NaOH)=2n(H2SO4),由于在溶液中c=![]() ,所以滴定时待测NaOH溶液浓度计算公式为:c(NaOH)=
,所以滴定时待测NaOH溶液浓度计算公式为:c(NaOH)=  。
。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】CO是合成尿素、甲酸的原料。
(1)在100 kPa和T K下,由稳定单质生成1 mol化合物的焓变称为该物质在T K时的标准摩尔生成焓,用符号ΔHθ表示。已知石墨和一氧化碳的燃烧热分别为393.5 kJ·mol-1和283.0 kJ·mol-1,则CO(g)的ΔHθ=_________。
(2)合成尿素的反应:2NH3(g)+CO(g)CO(NH2)2(g)+H2(g) ΔH=-81.0 kJ·mol-1;T℃时,在体积为2 L 的恒容密闭容器中,将2 mol的NH3和1 mol CO混合反应,5 min时,NH3的转化率为80%。则0~5 min平均反应速率为v(CO)=_________。
已知:
温度/K | 398 | 498 | … |
平衡常数(K) | 126.5 | K1 | … |
则:K1________(填“>”或“<”)126.5;其判断理由是__________。
(3)若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:
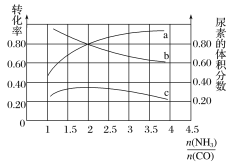
①若图中c表示平衡体系中尿素的体积分数,则a表示________的转化率。
②当![]() =________时,尿素含量最大;在该条件下,对于该反应既能增大反应速率又能使平衡正向移动的措施是_____(写一种)。
=________时,尿素含量最大;在该条件下,对于该反应既能增大反应速率又能使平衡正向移动的措施是_____(写一种)。