题目内容
17.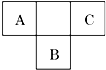 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B的最外层电子数是其电子层数两倍.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B的最外层电子数是其电子层数两倍.(1)写出A分子电子式
 .
.(2)B在元素周期表中的位置是第三周期第ⅥA族.
(3)C的原子结构示意图为
 .
.(4)比较B、C的原子半径:B>C,写出A的气态氢化物与B的最高价氧化物对应的水化物反应的化学方程式2NH3+H2SO4=(NH4)2SO4.
分析 根据A、C两元素的原子核外电子数之和等于B原子的质子数,原子核外电子数等于核内的质子数,设B的原子序数为x,则A的原子序数为x-9,y的原子序数为x-7,则有x-9+x-7=x,x=16,则B为S元素,符合:B的最外层电子数是其电子层数两倍,则A为N元素,C为F元素,根据元素所在周期表中的位置结合元素周期律知识解答该题.
解答 解:依据分析可知:A为氮,B为硫,C为氟,
(1)A为N,氮气为双原子分子,氮气的电子式为 ,故答案为:
,故答案为: ;
;
(2)B为S元素,原子序数为16,原子核外有3个电子层,最外层电子数为6,则位于周期表第三周期ⅥA族,
故答案为:第三周期第ⅥA族;
(3)C为F,原子核外有9个电子,最外层电子数为7,核内有9个质子,结构示意图为 ,
,
故答案为: ;
;
(4)S的原子半径大于O的原子半径,O原子半径大于F原子半径,故S>F,A的气态氢化物为NH3,B的最高价氧化物对应水化物为H2SO4,反应的化学方程式为2NH3+H2SO4=(NH4)2SO4,故答案为:>;2NH3+H2SO4=(NH4)2SO4.
点评 本题主要考查元素的位置结构性质的相互关系及应用,注意根据元素所在周期表中的位置和质子数的关系推断元素的种类,把握元素周期律的相似性和递变性的规律.

练习册系列答案
相关题目
7.下列说法均摘自某些科普杂志,你认为无科学性错误的是( )
| A. | 铅笔芯的原料是重金属铅,儿童在使用时不可以用嘴吮吸铅笔,以免引起铅中毒 | |
| B. | CO有毒,生有煤炉的居室放置数盆清水,这样可有效的吸收CO,防止煤气中毒 | |
| C. | 汽水浇灌农田有一定的道理,其中二氧化碳的缓释,有利于作物的光合作用 | |
| D. | 纯碱又名烧碱,成分是氢氧化钠 |
8.某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片、KSCN溶液.
实验记录(划斜线部分不必填写):
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:AEF.(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐被氧化在亚铁盐溶液中加入少量铁单质,并简述Fe2+的检验的方法取少量亚铁盐溶液加入几滴KSCN溶液无明显现象,通入氯水后溶液呈血红色.
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片、KSCN溶液.
实验记录(划斜线部分不必填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | Zn+Fe2+=Zn2++Fe | ||
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe3+具有氧化性 |
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:AEF.(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐被氧化在亚铁盐溶液中加入少量铁单质,并简述Fe2+的检验的方法取少量亚铁盐溶液加入几滴KSCN溶液无明显现象,通入氯水后溶液呈血红色.
5.下列实验操作中,正确的是( )
| A. | 稀释浓硫酸先在量筒中加一定体积水,再在不断搅拌下沿量筒壁慢慢加入浓硫酸 | |
| B. | 过滤时,漏斗里的滤液应低于滤纸的边缘 | |
| C. | 燃着的钠应立即用水灭火 | |
| D. | 测定溶液的pH值时,应用湿润玻棒蘸取待测液,直接滴在干燥的pH试纸上 |
12.某待测溶液中可能含有SO42-、SO32-、CO32-、HCO3-、NO3-、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出).
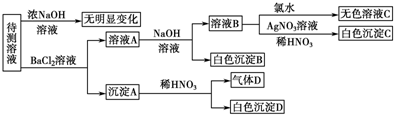
请回答下列问题:(1)根据上述框图信息填写下表(不能确定的不填):
(2)写出沉淀A三种可能的情况:BaSO3;BaSO3、BaSO4;BaCO3、BaSO4;BaCO3、BaSO3;BaSO3、BaCO3、BaSO4;,若气体D遇空气变红棕色,则生成沉淀D时肯定发生的反应的离子方程式为3BaSO3+2H++2NO3-═2NO↑+3BaSO4↓+H2O.
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是做焰色反应实验,观察到黄色火焰,则说明是钠.

请回答下列问题:(1)根据上述框图信息填写下表(不能确定的不填):
| 肯定存在的离子 | 肯定没有的离子 | |
| 化学式或离子符号 |
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是做焰色反应实验,观察到黄色火焰,则说明是钠.
9.“保护环境,就是保护自己.”目前,我国城市环境中主要的大气污染物是( )
| A. | HCl、NO2、N2、粉尘 | B. | CO2、Cl2、N2、雾 | C. | SO2、NO2、CO、烟尘 | D. | CO2、NO、NH3、H2S |
6.A、B为两短周期元素,A元素原子的L层比B元素原子的L层少3个电子,B原子核外电子总数比A原子核外电子总数多5,则A和B形成的化合物的化学式为( )
| A. | A2B3 | B. | BA2 | C. | AB4 | D. | B3A2 |
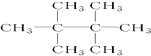 .
.