��Ŀ����
����Ŀ��ά����C��һ��ˮ����ά����(��ˮ��Һ������)�����Ļ�ѧʽ��C6H8O6������ȱ��������ά�����ܵû�Ѫ֢������ά����C�ֳƿ���Ѫ�ᡣ�����ʵ�ˮ�����߲ˡ�����Ʒ�ж�����ά����C���������ʳ�֭��ά����C�ĺ�����500mg/L���ҡ�ijУ����С��ⶨ��ij���ӵ�����װ��֭��ά����C�ĺ����������Dzⶨʵ��������档(����д�йؿհ�)
��һ���ⶨĿ�ģ��ⶨ����������װ��֭��ά����C�ĺ�����
�������ⶨԭ����C6H8O6+I2 ��C6H6O6+2H��+2I�D
������ʵ����Ʒ���Լ�
��1����������Ʒ(��ѡ����)
��2���Լ���ָʾ��___(������)��Ũ��Ϊ7.50��10��3mol��L-1��I2����Һ������ˮ�ȡ�
���ģ�ʵ�����
��1��ϴ�����������ζ����Ƿ�©Һ����ϴ��װ�ñ�����Һ���á�
��2����___(����������)����ƿ������20.00mL�����֭������2��ָʾ����
��3�������ֿ��Ƶζ��ܵ�___(�λ)������ҡ����ƿ���۾�ע��___��ֱ���ζ��յ㡣�ζ����յ�ʱ��������___��
���壩���ݼ�¼�봦��������������Ʋ��������ݼ�¼�����ݴ����ı����������ݣ���__

�������ݴ������ζ������ı�����Һ�������15.00mL����˳�֭��ά����C�ĺ�����___mg/L��
�������������ۣ�
��1���ζ�ʱ�ܷ����ҡ����ƿ��Ϊʲô��_____
��2���ӷ������ݿ���������װ��֭�Ƿ��Ǵ���Ȼ��֭��___(��ǡ����ǡ������ǡ�)������������ܲ�ȡ��������____(����)��
A����ˮϡ����Ȼ��֭ B����֭�ѱ�Ũ�� C����ά����C��Ϊ���Ӽ�
���𰸡�������Һ ��ʽ�ζ��ܣ�����Һ�ܣ� ���� ��ƿ����Һ��ɫ�仯 ��Һ��ɫ����ɫ���Ұ�����ڲ��ָ�ԭɫ
���� ��� | ��ʼ(mL) | �յ�(mL) | ��V |
1 | |||
2 | |||
3 |
990 ���ܣ���ֹҺ�彦�� ���� C
��������
(1)���ݵζ�ԭ��C6H8O6+I2 ��C6H6O6+2H��+2I�D���õ�Һ�ζ�ά����C��Һ���������۱�����
��2������ά����Cˮ��Һ������ѡ��������
��3�����ݵζ������Ĺ淶�ش𣻵������һ�ε�Һʱ����Һ��ʣ�ࣻ
��4���ζ�������Ҫ��¼�ζ��ܿ�ʼ���յ�Ŀ̶ȣ�ʵ���ظ�2-3�Σ�
��5�����ݷ�Ӧ����ʽC6H8O6+I2 ��C6H6O6+2H��+2I�D����˳�֭��ά����C�ĺ�����
��6������ҡ����ƿ��Һ��������
(7)������Ȼ��֭��ά����C�ĺ����жϣ�
(1)���ݵζ�ԭ��C6H8O6+I2 ��C6H6O6+2H��+2I�D���õ�Һ�ζ�ά����C��Һ������ѡ���ָʾ���ǵ�����Һ��
��2������ά����Cˮ��Һ�����ԣ�����ʽ�ζ��ܣ�����Һ�ܣ�����ƿ������20.00mL�����֭��
��3�������ֿ��Ƶζ��ܵĻ���������ҡ����ƿ���۾�ע����ƿ����Һ��ɫ�仯��ֱ���ζ��յ㡣�ζ����յ�ʱ�������ǵ������һ�ε�Һ��Һ����ɫ����ɫ���Ұ�����ڲ��ָ�ԭɫ��
��3���ζ�������Ҫ��¼�ζ��ܿ�ʼ���յ�Ŀ̶ȣ�ʵ���ظ�2-3�Σ�����Ϊ
���� ��� | ��ʼ(mL) | �յ�(mL) | ��V |
1 | |||
2 | |||
3 |
��
��5����20.00mL�����֭��ά����C�ĺ���Ϊxmol��
C6H8O6 + I2 �� C6H6O6 + 2H��+ 2I�D
1 1
7.50��10��3mol��L-1��0.015L x
X=1.125��10��4mol
�˳�֭��ά����C�ĺ�����![]() 0.99g/L=990mg/L��
0.99g/L=990mg/L��
��6��Ϊ��ֹҺ�彦�����ζ�ʱ���ܾ���ҡ����ƿ��
(7)���ʳ�֭��ά����C�ĺ�����500mg/L���ң���������װ��֭ά����C�ĺ�����990mg/L�����Բ��Ǵ���Ȼ��֭����ˮϡ����Ȼ��֭��ά����C�����ή�ͣ���֭�ѱ�Ũ��������˳ɱ�����ά����C��Ϊ���Ӽ������ά���صĺ�������ѡC��

 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д�����Ŀ����ҵ�ϳɰ���ӦΪNz(g)+3H2(g) ![]() 2NH3(g)�������о�����:��773 Kʱ���ֱ�2 mol N2��6 mol H2����һ���̶��ݻ�Ϊ1L ���ܱ������У����ŷ�Ӧ�Ľ��У�����������n(H2)��n(NH3)�뷴Ӧʱ��t�Ĺ�ϵ���±�;
2NH3(g)�������о�����:��773 Kʱ���ֱ�2 mol N2��6 mol H2����һ���̶��ݻ�Ϊ1L ���ܱ������У����ŷ�Ӧ�Ľ��У�����������n(H2)��n(NH3)�뷴Ӧʱ��t�Ĺ�ϵ���±�;
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n��H2��/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n��NH3��/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
(1) ǰ10min ������N2��ʾ�ķ�Ӧ����Ϊ________
(2) ���¶��£��˷�Ӧ��ƽ�ⳣ��K=__________
(3) ���¶��£�����ͬ�ݻ�����һ������Ͷ���N2��H2��NH3��Ũ�ȷֱ�Ϊ3 mol��L-1��3 mol��L-1��3 mol��L-1�����ʱv��_______v��(����>������<������=��)��
(4) ���¶��£�������ƽ����ϵ����ͨ��2molNH3��һ��ʱ��ﵽ�µ�ƽ�⡣��ʱc(H2)____ 4.5mo1/L(����>������<������=��)��
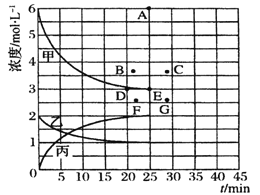
(5) ���ϱ��е�ʵ�����ݼ���õ���Ũ��-ʱ�����Ĺ�ϵ������ͼ�е����߱�ʾ����ʾc(N2)-t��������______���ڴ��¶��£�����ʼ����4 mol Nz ��12 mol Hz,��Ӧ�մﵽƽ��ʱ����ʾc(H2)-t����������Ӧ�ĵ�Ϊ_______��
����Ŀ����ͼ��ij��ͯ��Ԫ����챨�浥�IJ������ݣ��������ݣ��ش��������⣺
������ҽ�ƻ����ٴ����������浥 | ||||
������Ŀ | ����� | ��λ | �ο���Χ | |
1 | п(Zn) | 115.92 |
| 66~120 |
2 | ��(Fe) | 6.95�� |
| 7.52~11.82 |
3 | ��(Ca) | 1.68 |
| 1.55~2.10 |
(1)�ö�ͯ����_________Ԫ�غ���ƫ�͡�
(2)���浥������mol��L��1����__________(���������������������Ũ����)�ĵ�λ��
(3)����ά����C��ʹʳ���е�Fe3��ת��ΪFe2�������������������ά����C��________�ԡ�
(4)ȱ����ƶѪ����Ӧ����Fe2����һЩ����������������Ϊ��Ҫ�ɷ֣������������Ƴ�ҩƬʱ�������һ����������£��Ʋ����µ�������_______________________��
(5)ȡ��Ѫ��Ƭ���в���ϸ���������ϡ���ᣬȡ����Һ��Ȼ��μ�KSCN��Һ������Һ��Ϊ��ɫ������Һ�к���________(�����ӷ���)��˵����Ѫ���Ƿ����____________��