题目内容
【题目】请回答下列问题:
(1)近年来,人类生产、生活所产生的污染物,使雾霾天气逐渐增多。灰霾粒子比较小,平均直径大约在1000~2000nm左右。下列有关说法正确的是_____________
A.灰霾属于纯净物 B.雾霾天气,儿童、老年人应减少户外活动
C.灰霾能发生丁达尔现象 D.减少燃煤用量能降低灰霾天气的产生频率
(2)雾是由大量悬浮在近地面空气中的微小水滴或冰晶组成的气溶胶系统。雾丁达尔效应与水蒸汽有关,欲在树林中观察到丁达尔现象,你认为一天中最有可能观察到该现象的时间是____________,理由是___________________________________________________________
(3)为了消除SO2的污染,工业上采用石灰石-石膏湿法烟气脱硫工艺来降低含硫燃料燃烧排放的SO2。该技术的工作原理是使烟气中的SO2与浆液中的石灰石以及鼓入的空气反应生成生石膏(CaSO4·2H2O)。
①写出该工艺的化学方程式:______________________________________;该反应中每消耗标况下11.2L SO2,转移电子的物质的量为_____________
②若燃煤的含硫量(硫单质)为4%,燃烧1吨该燃煤生成的SO2有96%转化为生石膏,然后经过加热脱水形成熟石膏(2CaSO4·H2O),则可获得熟石膏_____________吨。
【答案】BD 清晨 小水滴或冰晶被太阳加热,形成水雾,可能构成1nm—100nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾时会产生丁达尔效应 2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2CO2 1mol 0.174
【解析】
(1)胶体的分散质粒子直径在1-100nm,已知灰霾平均直径大约在1000~2000nm左右,则灰霾不属于胶体,不具有胶体的性质;
(2)清晨小水滴或冰晶被太阳加热,形成水雾,可能构成1nm—100nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾时会产生丁达尔效应;
(3)①由题意可确定该原理的反应物、生成物,该反应为氧化还原反应,根据得失电子守恒、元素守恒配平方程式;计算出SO2物质的量,结合S元素化合价的变化,确定转移电子的物质的量;
②根据硫元素守恒进行计算。
(1)胶体的分散质粒子直径在1-100nm,灰霾粒子比较小,平均直径大约在1000~2000nm左右,则灰霾不属于胶体,不具有胶体的性质,
A. 灰霾是空气和固体颗粒形成的混合物,A项错误;
B. 雾霾是雾和霾的混合物,霾的核心物质是悬浮在空气中的烟、灰尘等物质,空气相对湿度低于80%,颜色发黄。气体能直接进入并粘附在人体下呼吸道和肺叶中,对人体健康有伤害,故雾霾天气,儿童、老年人应减少户外活动,B项正确;
C. 灰霾粒子比较小,平均直径大约在1000~2000nm左右,其粒子直径比可见光(400nm-700nm)大,不能发生光的散射,没有丁达尔现象,C项错误;
D. 减少燃煤用量能够减少有害气体以及烟尘的排放,能降低灰霾天气的产生频率,D项正确;
故答案为:BD;
(2)清晨小水滴或冰晶被太阳加热,形成水雾,可能构成1nm—100nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾时会产生丁达尔效应;
故答案为:清晨;清晨小水滴或冰晶被太阳加热,形成水雾,可能构成1nm—100nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾时会产生丁达尔效应;
(3)①为了消除SO2的污染,工业上采用石灰石-石膏湿法烟气脱硫工艺来降低含硫燃料燃烧排放的SO2,由题意知,该原理的反应物为CaCO3、SO2、O2、H2O,生成物为CaSO4·2H2O、CO2,该反应为氧化还原反应,根据得失电子守恒、元素守恒配平方程式为:2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2CO2;该反应每消耗标况下11.2L SO2,即0.5mol SO2,S元素化合价由+4价升高为+6价,则转移电子的物质的量为0.5mol×2=1mol;
故答案为:2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2CO2;1mol;
②S的物质的量为![]() ,由硫元素守恒可得,
,由硫元素守恒可得,![]() ,生石膏(CaSO4·2H2O)物质的量为:
,生石膏(CaSO4·2H2O)物质的量为:
![]() ,则熟石膏(2CaSO4·H2O)物质的量为
,则熟石膏(2CaSO4·H2O)物质的量为![]() ,则熟石膏(2CaSO4·H2O)的质量为
,则熟石膏(2CaSO4·H2O)的质量为![]() ;
;
故答案为:0.174。

 名校课堂系列答案
名校课堂系列答案【题目】【加试题】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲醛(在水中溶解度不大,易溶于有机溶剂,密度约等于水的密度)、苯甲酸。反应原理如下:
2C6H5CHO+NaOH![]() C6H5CH2OH+C6H5COONa
C6H5CH2OH+C6H5COONa
C6H5COONa+HCl![]() C6H5COOH+NaCl
C6H5COOH+NaCl
相关物质物理性质如下表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |
沸点/℃ | 178 | 205 | 249 | 80 |
熔点/℃ | 26 | -15 | 122 | 5.5 |
苯甲酸在水中的溶解度 | ||
17℃ | 25℃ | 100℃ |
0.21g | 0.34g | 5.9g |
实验流程如下:

(1)第Ⅰ步需连续加热1小时(如图1),其中加热混合固定装置为画出。
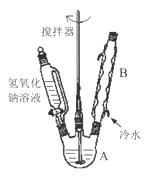
仪器A的名称为_______,若将仪器B改为仪器C,效果不如B,说明原因:_______。
(2)操作②有关分液漏斗的使用不正确的是_______
A.分液漏斗在使用之前必须检验是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时待下层液体放完后立即关闭旋塞,换掉烧杯再打开旋塞使上层液体流下
(3)操作③是用沸水浴加热蒸馏,再进行操作④(如图2),收集______℃的馏分。图2中有一处明显错误,正确的应改为_____________。
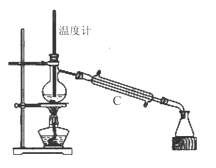
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体,用_____冲洗杯壁上残留的晶体。抽滤完成后用少量冰水对晶体进行洗涤,洗涤应____________。
(5)用电子天平准确称取0.2440g苯甲酸于锥形瓶中加100mL蒸馏水溶解(必要时可以加热),再用0.1000mol/L的标准氢氧化钠溶液滴定,共消耗标准氢氧化钠溶液19.20mL,苯甲酸的纯度为_____%。