题目内容
下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
| A、Mg(OH)2 |
| B、Al(OH)3 |
| C、SiO2 |
| D、SO2 |
考点:两性氧化物和两性氢氧化物
专题:元素及其化合物
分析:既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的铵盐(如(NH4)2CO3等)、弱酸的酸式盐(NaHCO3、NaHS等)、单质(如Al)、氨基酸、蛋白质等.
解答:
解:A.氢氧化镁与盐酸反应生成氯化镁与水,不能与氢氧化钠反应,故A错误;
B.氢氧化铝是两性氢氧化物,与盐酸反应生成氯化铝与水,与氢氧化钠反应生成偏铝酸钠与水,故B正确;
C.二氧化硅与氢氧化钠反应生成硅酸钠与水,不能与盐酸反应,故C错误;
D.二氧化硫与氢氧化钠反应生成亚硫酸钠与水,不能与盐酸反应,故D错误,
故选B.
B.氢氧化铝是两性氢氧化物,与盐酸反应生成氯化铝与水,与氢氧化钠反应生成偏铝酸钠与水,故B正确;
C.二氧化硅与氢氧化钠反应生成硅酸钠与水,不能与盐酸反应,故C错误;
D.二氧化硫与氢氧化钠反应生成亚硫酸钠与水,不能与盐酸反应,故D错误,
故选B.
点评:本题考查了元素化合物的性质,难度不大,明确物质的性质是解本题的关键,注意概念中学常见的既能与酸反应又能与碱反应的物质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O═Zn(OH)2+Mn2O3,下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、电池正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- |
| C、电池工作时,负极附近pH降低 |
| D、正极是水电离出的H+得到电子 |
短周期元素甲、乙、丙、丁的原子序数依次增大.甲的最高价氧化物与乙的氢化物同时通入水中得到的生成物既可与酸反应又可与碱反应.丙位于IA族,丁原子的核外电子总数是其最外层电子数的3倍,则( )
| A、气态氢化物的稳定性:乙>丁 |
| B、原子半径:甲<乙 |
| C、丙的两种氧化物都是离子化合物 |
| D、甲、乙、丁最高价氧化物对应水化物酸性依次增强 |
下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A、常温下都可用铁制容器贮存 |
| B、常温下都能与铜较快反应 |
| C、露置于空气中,溶液质量均减轻 |
| D、露置于空气中,溶液浓度均升高 |
下列各组物质的溶液不用其它试剂就可鉴别的是( )
| A、FeCl3 HCl NaCl NaOH |
| B、BaCl2 Na2CO3 HCl (NH4)2CO3 |
| C、HCl CuCl2 NaNO3 Na2SO4 |
| D、Na2CO3 Na2SO4 HCl H2SO4 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗先从下口放出下层液体,换一烧杯再从下口放出上层液体 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶有大量晶体析出时就应停止加热 |
| D、称量时,称量物置于托盘天平的左盘,砝码放在托盘天平的右盘 |
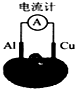 某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )
某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )| A、铝电极是该电池的负极 |
| B、电流由铜片通过导线流向铝片 |
| C、一段时间后,铜片质量会变小 |
| D、该电池将电能转化为了化学能 |
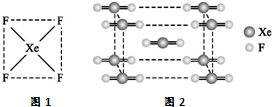 Ⅰ.自从英国化学家巴特列(N.Bartlett)首次合成了第一种稀有气体的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.
Ⅰ.自从英国化学家巴特列(N.Bartlett)首次合成了第一种稀有气体的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.