题目内容
25°C时,c(CH3COOH)+ c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、 c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是
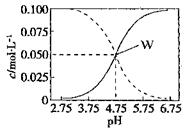

| A.pH=4的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+ c(H+)= c(CH3COOH)+c(OH-) |
| C.将W点所表示的1.0L溶液稀释到10L,用pH计测量,溶液的pH应为5.75 |
| D.pH=5.5的溶液中:c(Na+)+ c(H+)- c(OH-)+c(CH3COOH)=0.1mol/L |
C
试题分析:A、该溶液电离大于水解,呈酸性,正确;B、根据电荷守恒有c(Na+)+ c(H+)= c(CH3COO-)+c(OH-),该点有c(CH3COOH)=c(CH3COO-),故正确;C、W点处于醋酸的电离平衡和醋酸根的水解平衡的两个平衡体系,将此时1.0L溶液稀释到10L,稀释过程中会伴随醋酸的进一步电离和醋酸根的进一步水解,所以用pH计测量,溶液的pH不肯能为5.75,错误;D、将c(CH3COOH)+ c(CH3COO-)=0.1mol/L代入,该式为电荷守恒,正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
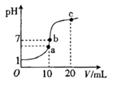
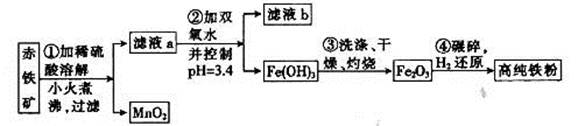
 Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
 Cu(OH) 2+2H+的平衡常数K=_______。
Cu(OH) 2+2H+的平衡常数K=_______。