题目内容
3.下列说法正确的是( )| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 含有离子键的化合物一定是离子化合物 | |
| C. | 含有共价键的物质一定是共价化合物 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
分析 A.离子化合物可能含有共价键;
B.含有离子键的化合物是离子化合物;
C.只含有共价键的化合物属于共价化合物;
D.分子的热稳定性由共价键决定.
解答 解:A.离子化合物一定有离子键,可能含有共价键,如NaOH属于离子化合物含有离子键和共价键,共价化合物中只含有共价键,故A错误;
B.含有离子键的化合物是离子化合物,离子化合物一定有离子键,可能含有共价键,故B正确;
C.只含有共价键的化合物属于共价化合物,含有共价键的化合物不一定是共价化合物,如NaOH属于离子化合物含有离子键和共价键,故C错误;
D.分子的热稳定性由共价键决定,分子间作用力决定物质的物理性质,故D错误.
故选B.
点评 本题考查离子键、共价键、离子化合物、共价化合物,熟悉概念是解答本题的关键,并注意利用实例来解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.在120℃条件下,1mL气态混合物与10mLO2混合后点燃,最终测得气体的总体积为11mL.则该气态混合物可能是( )
| A. | C2H4、C6H6 | B. | CH4、CH2O | C. | C3H8、CH3CH2OH | D. | C2H6、CH3CHO |
11.下列叙述正确的是( )
| A. | 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 | |
| B. | 将氢氧化钠溶液和氨水各稀释一倍,两者的c(OH-)均减少到原来的一半 | |
| C. | 常温下,某溶液中由水电离出的c(OH-)=1×10-10 mol/L,该溶液可能是盐酸 | |
| D. | 如果盐酸的物质的量浓度是醋酸的两倍,则盐酸的c(H+)也是醋酸的两倍 |
15.海洋水族馆中,表演者需携带氧气瓶在水中与鱼“共舞”.氧气被压缩在钢瓶中,其原因正确的是( )
| A. | 氧分子的大小发生改变 | B. | 氧分子的质量发生改变 | ||
| C. | 氧分子变成了氧原子 | D. | 氧分子之间的间隔变小了 |
13.下列叙述的原因不是由于原电池造成的是( )
| A. | 运输液氯的铁管被腐蚀 | B. | 金属在潮湿空气中更容易腐蚀 | ||
| C. | 铁与酸反应滴加硫酸铜后反应加快 | D. | 含杂质的锌比纯锌与酸反应快 |

 .
.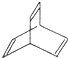 ,X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种.有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式:
,X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种.有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式: .
.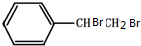 .
.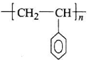 .
.