��Ŀ����
A��B��C��D���ֽ�������A��B��ϡ�������ԭ���ʱ��������������ΪB-��A����A��C�ֱ�Ͷ���Ũ�ȵ������У�C��A��Ӧ���ң��ö��Ե缫��⺬����ͬŨ�ȵ�B2+��D2+����Һʱ��D���ڵ缫����������A��B��C��D������������ǿ������˳��Ϊ��������
| A��A��B��D��C | B��A��B��C��D | C��C��D��A��B | D��C��A��B��D |
����������Խ���ã����ᷴӦԽ���ң��γ�ԭ���ʱ�������Ǵ����������������Խ�ǿ�������ȵõ��ӣ��������ӵ�������Խǿ����Ӧ�Ľ�������Խ�����ã��ݴ˻ش�
����⣺��A��B��ϡ�������ԭ���ʱ��������������ΪB-��A����A��ԭ��صĸ�������������A��B����A��C�ֱ�Ͷ���Ũ�ȵ������У�C��A��Ӧ���ң����Ի�������C��A���ö��Ե缫��⺬����ͬŨ�ȵ�B2+��D2+����Һʱ��D���ڵ缫�������������������B��D������֪�������Ļ�����˳����C��A��B��D��
��ѡD��
��ѡD��
�����������Խ����Ļ�ԵıȽ�Ϊ���忼��ԭ��غ͵���֪ʶ�������ڵ缫��Ӧ�ͷŵ�˳��Ŀ��飬ע�����ԭ��غ͵��صĹ���ԭ����ѧϰ��ע����ػ���֪ʶ�Ļ��ۣ��ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
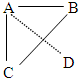 ��A��B��C��D����Ԫ��λ��Ԫ�����ڱ�������ͼ��ʾλ�ã���ش��������⣺
��A��B��C��D����Ԫ��λ��Ԫ�����ڱ�������ͼ��ʾλ�ã���ش��������⣺