题目内容
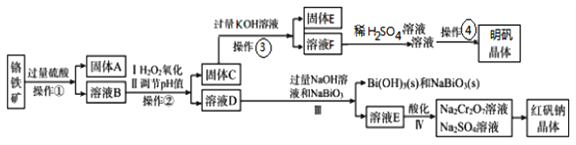
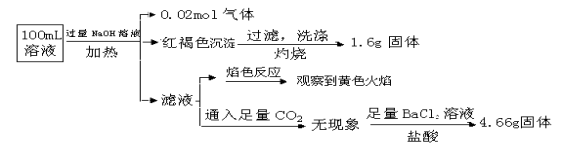
【题目】某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
下列说法正确的是( )
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol·L-1
C.SO42ˉ、NH4+ 、Na+一定存在,CO32ˉ一定不存在
D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+
【答案】B
【解析】
试题分析:①加入过量NaOH溶液,加热,得到0.02mol气体,说明有NH4+,而且为0.02mol。同时产生红褐色沉淀,说明有Fe3+,但由于Fe2+极易被氧化为Fe3+,所以这里不能排除原溶液中没有Fe2+存在,又由于Fe3+(或Fe2+)不能与CO32ˉ共存,所以原溶液中就没有CO32ˉ,且根据过滤、洗涤、灼烧后得1.6g固体(Fe2O3)可知Fe离子为0.02mol。②滤液焰色反应呈黄色,说明有Na+,但不能说明有原溶液中一定Na+,因为在加入过量NaOH溶液时,引入了Na+。③根据不溶于盐酸的4.66g沉淀,说明有SO42-,且为0.02mol。④根据电荷守恒可知一定有Cl-,且至少有0.02mol,因为如果原溶液中有Na+,则Cl-大于0.02mol,即c(Clˉ)≥0.2 mol·L-1。滤液中通入二氧化碳不产生沉淀,说明不存在铝离子。由此可知,原溶液中NH4+、SO42ˉ、Clˉ一定存在,Fe3+或Fe2+至少有一种存在;Na+可能存在也可能不存在;CO32ˉ、Al3+一定不存在,答案选B。

练习册系列答案
相关题目