题目内容
【题目】以红土镍矿(含NiO及铁、镁、硅的氧化物等)为原料制备Ni(OH)2的工艺流程如图:
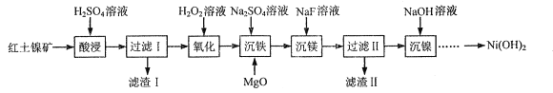
(1)“酸浸”时,H2SO4稍过量的目的是___。
(2)“氧化”时,Fe2+发生反应的离子方程式为___。
(3)“沉铁”时生成黄钠铣矾[Na2Fe6(SO4)4(OH)12]沉淀.该反应的化学方程式为___。
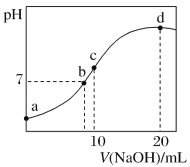
(4)“沉镁”时,需综合考虑镁去除率和镍损失率。不同pH下镁去除率和镍损失率如图所示。
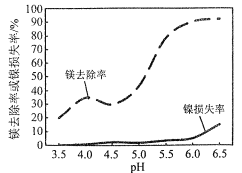
①应控制反应体系的pH约为___(填字母)。
A.5.0 B.6.0 C.6.5
②巳知Ksp(MgF2)=7.4×10-11。要使“沉镁”所得滤液中c(Mg2+)≤7.4×10-7mol·L-1,则应控制滤液中c(F-)不低于___。
(5)“沉镍”所得滤液中,可循环使用的主要溶质为___(填化学式)。
【答案】提高铁和镍元素的浸出率 2H++2Fe2++H2O2===2Fe3++2H2O 3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4 B 0.01mol·L—1 Na2SO4
【解析】
红土镍矿加硫酸溶液酸浸时,除硅的氧化物外,其他均溶解,因此滤渣1为硅的氧化物,而滤液1中含Fe2+、Mg2+和Ni2+,Fe2+被H2O2溶液氧化成Fe3+,沉铁时投入硫酸钠和氧化镁,发生反应3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4,再加NaF溶液沉镁后经过滤得到Mg(OH)2和[Na2Fe6(SO4)4(OH)12]的沉淀,所得滤液再加NaOH可得Ni(OH)2。
(1)“酸浸”时,H2SO4稍过量可提高铁和镍元素的浸出率,故答案为:提高铁和镍元素的浸出率;
(2)Fe2+被H2O2溶液氧化成Fe3+,反应方程式为:2H++2Fe2++H2O2===2Fe3++2H2O;
(3)根据上述分析,“沉铁”时生成黄钠铣矾[Na2Fe6(SO4)4(OH)12]的化学方程式为:3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4;
(4)根据图像可知,镁去除率最高和镍损失率最低的综合pH为6.5,故选B;
(5)Ksp(MgF2)=c(Mg2+)·c2(F—)=7.4×10-11,要使“沉镁”所得滤液中c(Mg2+)≤7.4×10-7mol·L-1,c2(F—) 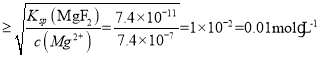 ,故答案为:0.01mol·L—1;
,故答案为:0.01mol·L—1;
(6)“沉镍”所得滤液中主要含Na2SO4,故循环利用的主要成分为Na2SO4。