题目内容
16.已知:共轭二烯烃(如1,3-丁二烯)可以发生如下两种加成反应:
请以苯酚为原料,其他无机试剂任选,合成
 ,写出正确的合成路线:
,写出正确的合成路线: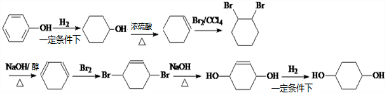 .
.
分析 以苯酚为原料,其他无机试剂任选,合成 ,先用苯酚和氢气发生加成反应生成环己醇,环己醇再和浓硫酸混合加热发生消去反应生成环己烯,环己烯和溴发生加成反应生成1,2-二溴环己烷,1,2-二溴环己烷和NaOH的醇溶液加热发生消去反应生成1,3-环己二烯,1,3-环己二烯和溴在较低温度下发生1,4加成生成1,4-二溴-2-环己烯,1,4-二溴-2-环己烯和NaOH的水溶液发生取代反应生成
,先用苯酚和氢气发生加成反应生成环己醇,环己醇再和浓硫酸混合加热发生消去反应生成环己烯,环己烯和溴发生加成反应生成1,2-二溴环己烷,1,2-二溴环己烷和NaOH的醇溶液加热发生消去反应生成1,3-环己二烯,1,3-环己二烯和溴在较低温度下发生1,4加成生成1,4-二溴-2-环己烯,1,4-二溴-2-环己烯和NaOH的水溶液发生取代反应生成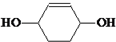 ,
, 和氢气发生加成反应生成
和氢气发生加成反应生成 ,据此分析解答.
,据此分析解答.
解答 解:以苯酚为原料,其他无机试剂任选,合成 ,先用苯酚和氢气发生加成反应生成环己醇,环己醇再和浓硫酸混合加热发生消去反应生成环己烯,环己烯和溴发生加成反应生成1,2-二溴环己烷,1,2-二溴环己烷和NaOH的醇溶液加热发生消去反应生成1,3-环己二烯,1,3-环己二烯和溴在较低温度下发生1,4加成生成1,4-二溴-2-环己烯,1,4-二溴-2-环己烯和NaOH的水溶液发生取代反应生成
,先用苯酚和氢气发生加成反应生成环己醇,环己醇再和浓硫酸混合加热发生消去反应生成环己烯,环己烯和溴发生加成反应生成1,2-二溴环己烷,1,2-二溴环己烷和NaOH的醇溶液加热发生消去反应生成1,3-环己二烯,1,3-环己二烯和溴在较低温度下发生1,4加成生成1,4-二溴-2-环己烯,1,4-二溴-2-环己烯和NaOH的水溶液发生取代反应生成 ,
, 和氢气发生加成反应生成
和氢气发生加成反应生成 ,其流程图为
,其流程图为 ,
,
故答案为: .
.
点评 本题考查有机物合成,为高考高频点,侧重考查学生知识运用能力,明确常见有机物官能团及其性质、常见反应类型、反应条件即可解答,可以根据目标采用采用逆向思维方法进行判断,题目难度中等.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
6.在下列各溶液中,离子可能大量共存的是( )
| A. | 无色的碱性溶液中:CrO42-、K+、Na+、SO42- | |
| B. | 使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量ClO-的溶液中:K+、H+、I-、SO42- | |
| D. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
4.下列关于卤化氢的说法不正确的是( )
| A. | 卤素原子半径越大,氢化物越稳定 | |
| B. | 卤素原子半径越大,氢化物越不稳定 | |
| C. | 卤素氢化物稳定性:HF>HCl>HBr>HI | |
| D. | 卤族单质与氢气越难反应,生成的氢化物越不稳定 |
11.下列各物质中,互为同系物的是( )
| A. |  与CH3-CH2-CH2-CH3 与CH3-CH2-CH2-CH3 | B. | 醋酸和十八酸 | ||
| C. | 乙二醇和甘油 | D. |  和 和 |
8.将足量的氯气通入下列溶液中,溶质阴、阳离子的数目都明显改变的是( )
| A. | AgNO3 | B. | FeBr2 | C. | NaOH | D. | Na2CO3 |
5.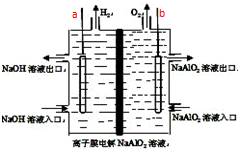 工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极),有关说法正确的是( )
工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极),有关说法正确的是( )
 工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极),有关说法正确的是( )
工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极),有关说法正确的是( )| A. | 当有0.1mol 电子发生转移时,a极产生气体在标准状况下为112mL | |
| B. | 该电池使用时应选择阴离子交换膜 | |
| C. | 电池工作结束后,左右两侧电解槽均会有Al(OH)3沉淀生成 | |
| D. | 该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑ |
 .
. As
As