题目内容
4.下列关于卤化氢的说法不正确的是( )| A. | 卤素原子半径越大,氢化物越稳定 | |
| B. | 卤素原子半径越大,氢化物越不稳定 | |
| C. | 卤素氢化物稳定性:HF>HCl>HBr>HI | |
| D. | 卤族单质与氢气越难反应,生成的氢化物越不稳定 |
分析 根据非金属强弱的比较依据:
1、同周期中,从左到右,随核电荷数的增加,原子半径逐渐减小,非金属性增强;同主族中,由上到下,随核电荷数的增加,原子半径逐渐增大,非金属性减弱;
2、依据最高价氧化物的水化物酸性的强弱:酸性愈强,其元素的非金属性也愈强;
3、依据其气态氢化物的稳定性:稳定性愈强,非金属性愈强;
4、与氢气化合的条件:越容易非金属性越强
解答 解:A、同主族中,由上到下,随核电荷数的增加,原子半径逐渐增大,非金属性减弱,氢化物越不稳定,故A错误;
B、同主族中,由上到下,随核电荷数的增加,原子半径逐渐增大,非金属性减弱,氢化物越不稳定,故B正确;
C、同主族中,由上到下,随核电荷数的增加,非金属性减弱,卤化氢稳定性为HF>HCl>HBr>HI,故C正确;
D、同主族中,由上到下,随核电荷数的增加,非金属性减弱,与氢气越难反应,生成物越不稳定,故D正确;
故选:A.
点评 抓住非金属性越强,与氢气越容易反应,生成物越稳定,注意元素周期表中多变规律的应用是关键,难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
14.能与NaOH溶液反应的含共价键的化合物是( )
| A. | 金刚石 | B. | 晶体硅 | C. | 石英(SiO2) | D. | MgO |
12.将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL 4.40mol/L盐酸中,充分反应后产生896mL H2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L.则原混合物中单质铁的质量是( )
| A. | 2.24g | B. | 3.36g | C. | 5.60g | D. | 10.08g |
19.下列说法不正确的是( )
| A. | 使用可再生资源、用超临界二氧化碳替代有机溶液剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 | |
| B. | 煤的干馏得到的煤焦油中可以分离出苯及其同系物,也可以分离出乙烯、丙烯等石油化工原料 | |
| C. | 用原子吸收光谱可以确定物质中含有哪些金属元素 | |
| D. | 淀粉、麦芽糖糖水解后的最终产物都是葡萄糖 |
9.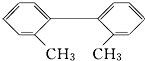 已知C-C键可以绕键轴自由旋转,对于结构简式为如图所示的烃,下列说法中正确的是( )
已知C-C键可以绕键轴自由旋转,对于结构简式为如图所示的烃,下列说法中正确的是( )
 已知C-C键可以绕键轴自由旋转,对于结构简式为如图所示的烃,下列说法中正确的是( )
已知C-C键可以绕键轴自由旋转,对于结构简式为如图所示的烃,下列说法中正确的是( )| A. | 分子中至少有8个碳原子处于同一平面上 | |
| B. | 分子中至少有9个碳原子处于同一平面上 | |
| C. | 该烃苯环上的一氯取代物最多有四种 | |
| D. | 该烃是苯的同系物 |
13.能证明丙烯分子里含有一个碳碳双键的事实是( )
| A. | 丙烯分子里碳氢原子个数比为1:2 | |
| B. | 丙烯完全燃烧生成的CO2和H2O的物质的量相等 | |
| C. | 丙烯容易与溴水发生加成反应,且1mol乙烯完全加成消耗1mol溴单质 | |
| D. | 丙烯能使酸性KMnO4溶液褪色 |


 ,写出正确的合成路线:
,写出正确的合成路线: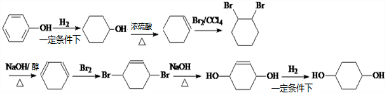 .
.