题目内容
下列各组热化学方程式(同温、同压下)中 大于
大于 (
( 、
、 为热量的数值)的是( )
为热量的数值)的是( )
A.①② B.③④ C.②④ D.①③
 大于
大于 (
( 、
、 为热量的数值)的是( )
为热量的数值)的是( )①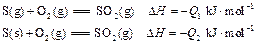 | ②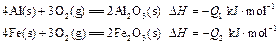 |
③ | ④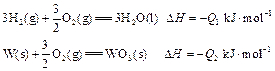 |
A
略

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
题目内容
 大于
大于 (
( 、
、 为热量的数值)的是( )
为热量的数值)的是( )①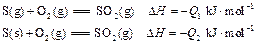 | ②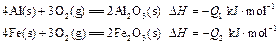 |
③ | ④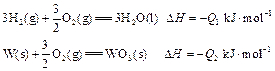 |

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案