题目内容
【题目】镇痛药物![]() 的合成方法如下:
的合成方法如下:
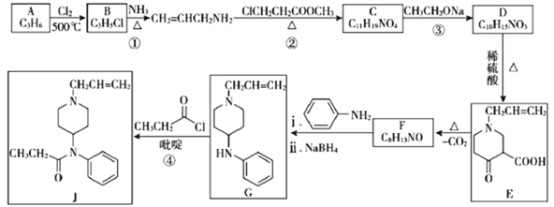
已知:
(1)![]() 的名称为_________________;②的反应类型为_________________反应。
的名称为_________________;②的反应类型为_________________反应。
(2)![]() 的结构简式为_________________.
的结构简式为_________________.![]() 中含氧官能团的名称为_________________.
中含氧官能团的名称为_________________.
(3)③的化学方程式为__________________________________。
(4)有机物![]() 分子组成比
分子组成比![]() 少两个氢原子,符合下列要求的
少两个氢原子,符合下列要求的![]() 的同分异构体有_________种。
的同分异构体有_________种。
A 遇![]() 显紫色 B 苯环上有两个取代基
显紫色 B 苯环上有两个取代基
(5)已知④有一定的反应限度,反应进行时加入吡啶(![]() ,属于有机碱)能提高
,属于有机碱)能提高![]() 的产率,原因是___________________________________________________。
的产率,原因是___________________________________________________。
(6)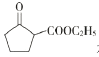 ,是一种重要的化工中间体。以环己醇(
,是一种重要的化工中间体。以环己醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出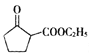 的合成路线。
的合成路线。
(已知:![]()
![]() 、
、![]() 为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________________________________
为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________________________________
【答案】3-氯丙烯(或3-氯-1-丙烯) 取代反应 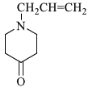 羰基
羰基 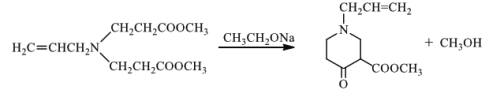 15 吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率
15 吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率 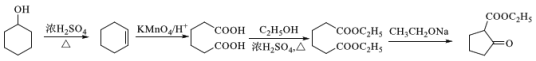
【解析】
由![]() 逆推,可知B是
逆推,可知B是![]() 、A是
、A是![]() ;
;
![]() ,结合
,结合![]() ,可知C是
,可知C是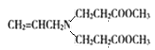 ;由
;由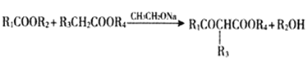 ,
,![]() ,则D是
,则D是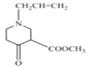 ,D在稀硫酸中水解为E
,D在稀硫酸中水解为E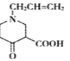 ;根据
;根据 ,逆推F为
,逆推F为![]() 。
。
根据上述分析可知,
(1)有机物A为CH2=CH-CH3,与氯气在500℃发生取代反应生成CH2=CH-CH2Cl(B),其名称为3-氯丙烯(或3-氯-1-丙烯);结合给定信息可知②的反应类型为取代反应,
故答案为:3-氯丙烯(或3-氯-1-丙烯);取代反应;
(2)对照有机物E结构简式,结合有机物F的分子式可知,有机物E→F脱去二氧化碳,去掉COO,得到F结构简式为 ;依据官能团的结构特点可知,F中含氧官能团名称为羰基;
;依据官能团的结构特点可知,F中含氧官能团名称为羰基;
故答案为: 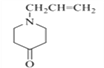 ;羰基;
;羰基;
(3)根据题给信息可知:有机物C在乙醇钠条件下,发生反应生成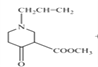 ;所以③化学方程式为
;所以③化学方程式为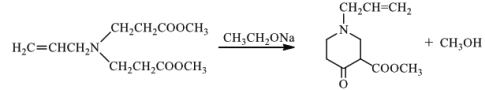 ;
;
故答案为: 。
。
(4)有机物F为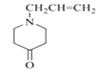 ,有机物K分组成比F少两个氢原子,分子式为C8H11NO,a.遇FeCl3显紫色,含有酚羟基;b.苯环上有两个取代基,一个必须是酚羟基;具体结构如下:苯环上分别连有-OH 和-CH2CH2-NH2 结构有3种;苯环上分别连有-OH 和 CH3CH(NH2)-结构有3种;苯环上分别连有-OH 和CH3-NH-CH2-结构有3种;苯环上分别连有-OH 和CH3CH2NH- 结构有3种;苯环上分别连有-OH 和(CH3)2N- 结构有3种;共计有15种;
,有机物K分组成比F少两个氢原子,分子式为C8H11NO,a.遇FeCl3显紫色,含有酚羟基;b.苯环上有两个取代基,一个必须是酚羟基;具体结构如下:苯环上分别连有-OH 和-CH2CH2-NH2 结构有3种;苯环上分别连有-OH 和 CH3CH(NH2)-结构有3种;苯环上分别连有-OH 和CH3-NH-CH2-结构有3种;苯环上分别连有-OH 和CH3CH2NH- 结构有3种;苯环上分别连有-OH 和(CH3)2N- 结构有3种;共计有15种;
故答案为:15;
(5) 吡啶(C5H5N,属于有机碱),吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率;
故答案为:吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率;
(6) ![]() 发生消去生成环己烯,环己烯酸性被高锰酸钾溶液氧化为HOOC-CH2-CH2-CH2-CH2-COOH,该有机物再与乙醇发生酯化反应生成CH3CH2OOC-CH2-CH2-CH2-CH2-COOCH2CH3,最后根据信息
发生消去生成环己烯,环己烯酸性被高锰酸钾溶液氧化为HOOC-CH2-CH2-CH2-CH2-COOH,该有机物再与乙醇发生酯化反应生成CH3CH2OOC-CH2-CH2-CH2-CH2-COOCH2CH3,最后根据信息 ,CH3CH2OOC-CH2-CH2-CH2-CH2-COOCH2CH3在乙醇钠的条件下发生反应生成
,CH3CH2OOC-CH2-CH2-CH2-CH2-COOCH2CH3在乙醇钠的条件下发生反应生成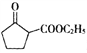 ;合成流程如下:
;合成流程如下: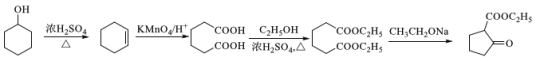 ;正确答案:
;正确答案: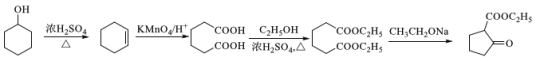 。
。

 名校课堂系列答案
名校课堂系列答案【题目】甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H—H | C—O | C≡O | H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=__________kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=_________kJ·mol-1
(2)反应①的化学平衡常数K的表达式为_______________;③的化学平衡常数K的表达式为_____________;