题目内容
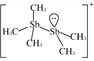
【题目】有关分子结构 ![]() 的下列叙述中,正确的是
的下列叙述中,正确的是
A.可能在同一平面上的原子最多有20个
B.12个碳原子不可能都在同一平面上
C.所有的原子都在同一平面上
D.除苯环外的其余碳原子有可能都在一条直线上
【答案】A
【解析】
试题分析:A.![]() 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子(或一个氟原子)共平面,则两个甲基有2个氢原子(或一个氟原子)可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故A正确; B.
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子(或一个氟原子)共平面,则两个甲基有2个氢原子(或一个氟原子)可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故A正确; B.![]() 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面,故B错误;C.甲烷是正四面体结构,分子中含有甲基,所有的原子不可能都在同一平面上,故C错误;D.乙烯是平面结构,不是直线结构,其余碳原子不可能都在一条直线上,故D错误,故选A。
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面,故B错误;C.甲烷是正四面体结构,分子中含有甲基,所有的原子不可能都在同一平面上,故C错误;D.乙烯是平面结构,不是直线结构,其余碳原子不可能都在一条直线上,故D错误,故选A。

 名校课堂系列答案
名校课堂系列答案【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
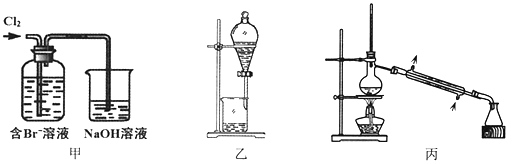
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2
【题目】为测定铝热反应实验所得“铁块”的成分,某学生兴趣小组设计实验流程如图所示。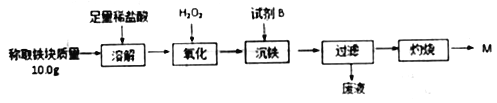
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
(1)取溶解操作得到的溶液,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因,除了可能混有没反应完的氧化铁外,还有一个原因是_______________。
(2)沉铁操作应调节溶液pH的范围的为________,试剂B 选择______。(填序号)
a.稀盐酸 b.氧化铁 c.MgCO3固体 d.氨水
(3)已知常温下Fe(OH)3的Ksp=1.1×10-36,则铁完全沉淀时溶液中c(Fe3+)=_____mol/L。
(4)根据流程得到的固体M质量_____(填“能”或“不能”)计算出铁块中金属铁的质量,原因是________________。
(5)另有小组采用滴定的方式测定“铁块”中铁的含量(铁元素只存在Fe和Fe2O3),测定方式如下:
I.取10g“铁块”粉碎,加入足量氢氧化钠溶液充分反应,过滤、洗涤、干燥,得到8.88g固体。将固体加入足量盐酸溶解,获得200mL溶液A;
II.取出10mL 溶液A 于锥形瓶,先加入足量的SnCl2溶液,将Fe3+全部转化为Fe2+,除去过量的Sn2+;
III.加入一定量的硫酸和磷酸,并滴加指示剂。再向锥形瓶中滴加0.1000mol/LK2Cr2O7溶液,恰好完全反应时,共消耗12.50mL K2Cr2O7溶液。发生反应:Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O
①步骤I中加入足量氢氧化钠溶液的作用为________________________。
②请计算样品中Fe单质的质量分数__________(写出计算过程)。