题目内容
下列方程式书写正确的是( )
| A、醋酸和氨水恰好完全中和:CH3COOH+NH3?H2O═CH3COO-+NH4++H2O |
| B、氢溴酸溶于水中:HBr?H++Br- |
| C、Na2CO3溶液中:CO32-+2H2O?H2CO3+2OH- |
| D、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(I):△H=-285.8kJ/mol |
考点:离子方程式的书写,热化学方程式
专题:离子反应专题,化学反应中的能量变化
分析:A.醋酸和氨水恰好完全中和生成醋酸铵和水,注意醋酸和一水合氨为弱电解质,保留化学式;
B.氢溴酸为强电解质,电离用等号;
C.碳酸根离子为多元弱酸根离子,分步水解;
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量.
B.氢溴酸为强电解质,电离用等号;
C.碳酸根离子为多元弱酸根离子,分步水解;
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量.
解答:
解:A.醋酸和氨水恰好完全中和:CH3COOH+NH3?H2O═CH3COO-+NH4++H2O,故A正确;
B.氢溴酸溶于水,电离的方程式为:HBr=H++Br-,故B错误;
C.Na2CO3溶液中,碳酸根离子的水解离子方程式为:CO32-+H2O?HCO3-+OH-,故C错误;
D.氢气燃烧的热化学方程式表示为:H2(g)+
O2(g)═H2O(l)△H=-285.8kJ/mol,故D错误;
故选:A.
B.氢溴酸溶于水,电离的方程式为:HBr=H++Br-,故B错误;
C.Na2CO3溶液中,碳酸根离子的水解离子方程式为:CO32-+H2O?HCO3-+OH-,故C错误;
D.氢气燃烧的热化学方程式表示为:H2(g)+
| 1 |
| 2 |
故选:A.
点评:本题考查了离子方程、热化学方程式的书写,书写电离方程式时应注意判断电解质的强弱,书写多元弱酸盐水解离子方程式时应注意分步水解,书写物质燃烧的热化学方程式应注意物质的物质的量为1mol,反应生成的物质为稳定的氧化物.

练习册系列答案
相关题目
下列说法错误的是( )
| A、SO2通入BaCl2溶液中无沉淀产生,通入FeCl3和BaCl2的混合溶液中有白色沉淀生成 |
| B、红磷在氯气中燃烧产生白色烟雾 |
| C、氯化碘(ICl)的化学性质与氯气相似,它跟水反应可生成HI和HClO |
| D、可在NaOH溶液液面上用倒扣漏斗装置吸收残余氯气 |
等质量的氢气在足量的氧气中燃烧,生成水蒸气时放出热量Q1,生成液态水时放出热Q2,则Q1与Q2的关系是( )
| A、Q1>Q2 |
| B、Q1<Q2 |
| C、Q1=Q2 |
| D、无法确定 |
下列物质在一定条件下,可与CH4发生取代反应的是( )
| A、氧气 |
| B、液溴 |
| C、氯气 |
| D、酸性KMnO4溶液 |
钠多以资源丰富的NaCl为原料来制备,下列方法中能够制备出金属钠的是( )
| A、加热NaCl晶体 |
| B、用金属钾置换出NaCl溶液中Na+ |
| C、电解NaCl溶液 |
| D、电解熔融的NaCl |
某粒子M的结构示意图为 ,下列有关该粒子的说法中不正确的是( )
,下列有关该粒子的说法中不正确的是( )
 ,下列有关该粒子的说法中不正确的是( )
,下列有关该粒子的说法中不正确的是( )| A、x值有6种以上的可能 |
| B、M粒子的符号可能是O2-、Ne、Al3+等 |
| C、M粒子表示的阴离子中还原性最弱的是N3- |
| D、取含有M粒子的溶液进行焰色反应,若为黄色,则M的符号是Na+ |
下列有关实验装置的说法中正确的是( )
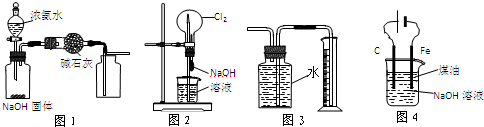

| A、图1装置可制取干燥纯净的NH3 |
| B、图2装置可以完成“喷泉”实验 |
| C、图3装置可测量Cu与浓硝酸反应产生气体的体积 |
| D、图4装置可用于实验室制备Fe(OH)2 |
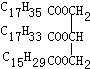 某油脂常温呈液态,其中一种成分的结构简式如图:
某油脂常温呈液态,其中一种成分的结构简式如图: