题目内容
A是芳香烃的含氧衍生物.为了测定其分子组成,进行如下实验:
①在一定温度和压强下将A气化,其气体的质量是同温、同压下等体积氦气质量的38倍;
②称取7.6gA,在11.2L氧气中完全燃烧,其产物只有CO2和水蒸气.将反应后的混合气通过浓硫酸后体积为10.64L,浓H2SO4质量增加3.6g.再将余下的气体通过盛有足量Na2O2的干燥管后,气体体积减少至6.16L(气体体积均在标准状况下测定).试回答:
(1)A的分子式为 ;
(2)A物质苯环上只有一取代基,遇FeCl3溶液无显色反应.1mol A只能与1mol NaHCO3反应;1mol A与足量Na反应生成1mol H2.则A的结构简式为 ;
(3)A与足量钠反应的化学方程式是 .
①在一定温度和压强下将A气化,其气体的质量是同温、同压下等体积氦气质量的38倍;
②称取7.6gA,在11.2L氧气中完全燃烧,其产物只有CO2和水蒸气.将反应后的混合气通过浓硫酸后体积为10.64L,浓H2SO4质量增加3.6g.再将余下的气体通过盛有足量Na2O2的干燥管后,气体体积减少至6.16L(气体体积均在标准状况下测定).试回答:
(1)A的分子式为
(2)A物质苯环上只有一取代基,遇FeCl3溶液无显色反应.1mol A只能与1mol NaHCO3反应;1mol A与足量Na反应生成1mol H2.则A的结构简式为
(3)A与足量钠反应的化学方程式是
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)在一定温度和压强下将A汽化,其质量是同温、同压下氦气质量的38倍,则A的相对分子质量是38×4=152,7.6g有机物A的物质的量是0.05mol,浓硫酸增重3.6g,则反应中生成的水的质量是3.6g,物质的量的是0.2mol,再将余下的气体通过盛有足量Na2O2的干燥管,气体体积减少至6.16L(气体体积均在标准状况下测定),由方程式:2Na2O2+2CO2=2Na2CO3+O2,可知生成的CO2是(10.64L-6.16L)×2=8.96L,物质的量是8.96L÷22.4L/mol=0.4mol,则根据原子守恒可知,A中碳氢原子的个数分别是8、8,所以氧原子的个数是
=3,因此化学式是C8H8O3,
(2)A物质遇FeCl3溶液无显色反应,说明分子中没有酚羟基,1mol A只能与1mol NaHCO3反应,1mol A与足量Na反应生成1mol H2,说明分子中含1个醇羟基和1个羧基,A物质苯环上只有一取代基,故侧链为-CH(OH)COOH;
(3)醇羟基、羧基都与Na反应生成氢气.
| 152-96-8 |
| 16 |
(2)A物质遇FeCl3溶液无显色反应,说明分子中没有酚羟基,1mol A只能与1mol NaHCO3反应,1mol A与足量Na反应生成1mol H2,说明分子中含1个醇羟基和1个羧基,A物质苯环上只有一取代基,故侧链为-CH(OH)COOH;
(3)醇羟基、羧基都与Na反应生成氢气.
解答:
解:(1)Mr(A)=38×Mr(He)=38×4=152,7.6gA的物质的量=
=0.05mol,
浓硫酸增重3.6g,则反应中生成的水的质量是3.6g,n(H)=
×2=0.4mol,
再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至6.16L(气体体积均在标准状况下测定),则:
2Na2O2+2CO2=2Na2CO3+O2,体积减小
2 1
(10.64L-6.16L)×2 10.64L-6.16L
可知生成的CO2是(10.64L-6.16L)×2=8.96L,物质的量是8.96L÷22.4L/mol=0.4mol,
则根据原子守恒可知,A分子中碳原子数目=
=8、氢原子数目═
=8,所以氧原子的个数是
=3,因此A的分子式是C8H8O3,
故答案为:C8H8O3;
(2)A的分子式是C8H8O3,A物质遇FeCl3溶液无显色反应,说明分子中没有酚羟基,1mol A只能与1mol NaHCO3反应,1mol A与足量Na反应生成1mol H2,说明分子中含1个醇羟基和1个羧基,A物质苯环上只有一取代基,故侧链为-CH(OH)COOH,故A的结构简式为: ,
,
故答案为: ;
;
(3)醇羟基、羧基都与Na反应生成氢气,A与足量钠反应的化学方程式是: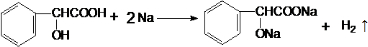 ,
,
故答案为: .
.
| 7.6g |
| 152g/mol |
浓硫酸增重3.6g,则反应中生成的水的质量是3.6g,n(H)=
| 3.6g |
| 18g/mol |
再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至6.16L(气体体积均在标准状况下测定),则:
2Na2O2+2CO2=2Na2CO3+O2,体积减小
2 1
(10.64L-6.16L)×2 10.64L-6.16L
可知生成的CO2是(10.64L-6.16L)×2=8.96L,物质的量是8.96L÷22.4L/mol=0.4mol,
则根据原子守恒可知,A分子中碳原子数目=
| 0.4mol |
| 0.05mol |
| 0.4mol |
| 0.05mol |
| 152-96-8 |
| 16 |
故答案为:C8H8O3;
(2)A的分子式是C8H8O3,A物质遇FeCl3溶液无显色反应,说明分子中没有酚羟基,1mol A只能与1mol NaHCO3反应,1mol A与足量Na反应生成1mol H2,说明分子中含1个醇羟基和1个羧基,A物质苯环上只有一取代基,故侧链为-CH(OH)COOH,故A的结构简式为:
 ,
,故答案为:
 ;
;(3)醇羟基、羧基都与Na反应生成氢气,A与足量钠反应的化学方程式是:
 ,
,故答案为:
 .
.
点评:本题考查有机物的推断,属于计算型推断,是高考中常见题型,试题综合性强,在注重对学生基础知识巩固和训练的同时,旨在培养学生分析、归纳、总结问题的能力,有利于培养学生的逻辑推理能力和创新思维能力,该题的关键是利用好守恒法,难度中等.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
已知H2SO4电离方程式是:H2SO4=H++HSO4-,HSO4-?H++SO42-,又知0.1mol?L-1 NaHSO4溶液的pH=2.则下列说法不正确的是( )
| A、Na2SO4溶液显碱性是因为SO42-+H2O?HSO4-+OH- |
| B、在NaHSO4溶液中,显酸性是因为HSO4-的电离 |
| C、NaHSO4溶液中各种离子浓度的关系是c(Na+)>c(HSO4-)>c(H+)>c(SO42-)>c(OH- ) |
| D、0.1mol?L-1 H2SO4溶液中氢离子的物质的量浓度为0.11mol?L-1 |
下列方程式书写正确的是( )
| A、醋酸和氨水恰好完全中和:CH3COOH+NH3?H2O═CH3COO-+NH4++H2O |
| B、氢溴酸溶于水中:HBr?H++Br- |
| C、Na2CO3溶液中:CO32-+2H2O?H2CO3+2OH- |
| D、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(I):△H=-285.8kJ/mol |
将a molNa2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应.当排出气体为两种气体时,a:b的值不可能是( )
| A、1:1 | B、1:2 |
| C、2:3 | D、3:2 |



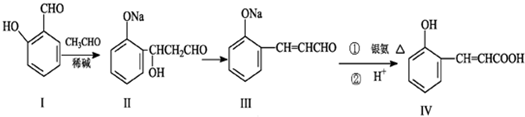
 .
.