题目内容
4.相同温度和压强下,在容积为2L的密闭容器中发生反应:2HI(g)?H2(g)+I2(g),达到平衡状态的标志是( )| A. | 颜色保持不变 | |
| B. | 气体密度保持不变 | |
| C. | 2v正(HI)=v逆(I2) | |
| D. | 拆开2 mol H-I共价键,同时生成1 mol H-H共价键 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、混合气体的颜色不再变化,说明碘蒸气的浓度不变,反应达到平衡状态,故A正确;
B、定容密闭容器中,混合气体的质量和条件不变,密度始终恒定不变,不能说明反应达到平衡状态,故B错误;
C、速率之比等于化学方程式计算之比,为正反应速率之比,2v正(HI)=v逆(I2)不符合速率之比等于化学方程式计算数之比,故C错误;
D、单位时间内拆开2molH-I共价键,同时生成1mol H-H,都是正向反应,不能确定 正逆反应速率相等,不能确定达到了平衡状态,故D错误;
故选A.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征,注意当反应达到平衡状态时,正逆反应速率相等,

练习册系列答案
相关题目
14.由与Ne原子电子层结构相同的离子和与Ar原子电子层结构相同的离子所形成的离子化合物是( )
| A. | MgCl2 | B. | K2S | C. | LiCl | D. | Na2O |
15.下列物质通入或加入溴水后,不是因发生化学反应而使溴水褪色的是( )
| A. | SO2 | B. | C2H4 | C. | 苯 | D. | NaOH |
12.下列组合中中心离子的电荷数和配位数均相同的是( )
| A. | K[Ag(CN)2]、[Cu(NH3)4]SO4 | B. | [Ag(NH3)2]Cl、K[Ag(CN)2] | ||
| C. | [Ag(NH3)2]Cl、[Cu(NH3)4]SO4 | D. | [Ni(NH3)4]Cl2、[Ag(NH3)2]Cl |
16.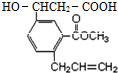 某有机物的结构简式如图所示,该有机物可能发生的反应是( )
某有机物的结构简式如图所示,该有机物可能发生的反应是( )
①酯化反应;②银镜反应;③加成反应;④取代反应;⑤氧化反应;⑥加聚反应;⑦缩聚反应;⑧水解反应.
 某有机物的结构简式如图所示,该有机物可能发生的反应是( )
某有机物的结构简式如图所示,该有机物可能发生的反应是( )①酯化反应;②银镜反应;③加成反应;④取代反应;⑤氧化反应;⑥加聚反应;⑦缩聚反应;⑧水解反应.
| A. | ①③④⑤⑥⑦⑧ | B. | ①②③④⑤⑥⑧ | C. | ①②③⑥⑧ | D. | ①③④⑤⑥⑧ |
13.下列说法正确的是( )
| A. | 铝合金是目前用量最大、用途最广的合金 | |
| B. | 二氧化硫使品红溶液褪色和使溴水褪色的原理相同 | |
| C. | 三种分散系中,胶体的稳定性介于溶液和浊液之间,属于介稳体系 | |
| D. | 活泼金属在空气中易与氧气反应,表面生成一层氧化物,对内部金属都能起保护作用 |
 3,3,4,6-四甲基辛烷
3,3,4,6-四甲基辛烷 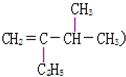 3-甲基-2-乙基-1-丁烯
3-甲基-2-乙基-1-丁烯  2,6-二甲基乙苯.
2,6-二甲基乙苯.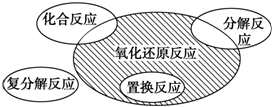 氧化还原反应和离子反应是中学化学中重要的反应类型.回答下列问题:
氧化还原反应和离子反应是中学化学中重要的反应类型.回答下列问题: =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O
