题目内容
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·molˉ1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成 AlN 的总热化学方程式是___________________;
(2) “亚硫酸盐法”吸收烟气中的SO2,室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。
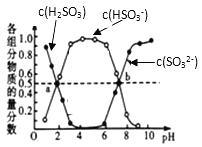
请写出a点时n(HSO3-)∶n(H2SO3)=______,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=______;
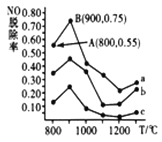
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO![]() 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
①请写出N2的电子式________;
② 曲线c对应NH3与NO的物质的量之比是______;
③曲线a中NO的起始浓度为6×10-4mg·m-3,从A点到B点经过0.8s,该时间段内NO的脱除速率为___________mg·m-3·s-1;
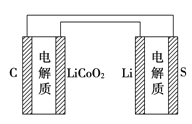
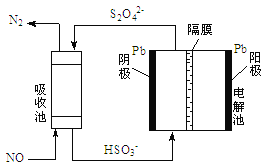
(4)间接电化学法可除NO。其原理如上右图所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)__________________。
【答案】Al2O3(s)+3C(s)+N2(g)═2AlN(s)+3CO(g)△H=+1026kJ/mol 1:1 3:1 ![]() 1:3 1.5×10-4 2HSO3-+2H++2e-=S2O42-+2H2O
1:3 1.5×10-4 2HSO3-+2H++2e-=S2O42-+2H2O
【解析】
(1)2C(s)+O2(g)=2CO(g) △H1=-221kJ/mol ①
4Al(g)+3O2(g)=2Al2O3(s) △H2=-3351kJ/mol ②
2Al(g)+N2(g)=2AlN(s) △H3=-318kJ/mol ③
将方程式(3①-②)×1/2+③得Al2O3(s)+3C(s)+N2(g)═2AlN(s)+3CO(g),△H=[3(-221kJ/mol)-(-3351kJ/mol)]×1/2+(-318 kJ/mol)=+1026kJ/mol,
(2)根据图知,a点溶液中c(HSO3-)=c(H2SO3),溶液体积相同,所以存在n(HSO3-):c(H2SO3)=1:1;b点溶液中c(HSO3-)=c(SO32-)=1,溶液中存在电荷守恒c(OH-)+c(HSO3-)+2c(SO32-)=c(NH4+)+c(H+),溶液的pH=7,则c(OH-)=c(H+),则c(HSO3-)+2c(SO32-)=c(NH4+),溶液体积相同,所以n(NH4+):n(HSO3-)=3:1,
故答案为:1:1;3:1;
(3)①氮气分子中N原子之间共用3个电子对,每个N原子含有1个孤电子对,电子式为![]() ;
;
②氨气的物质的量越多,NO的去除率越大,c曲线中NO脱除率最低,说明NO的物质的量最多,则n(NH3):n(NO)=1:3;
③曲线a中NO的起始浓度为6×10-4mgm-3,NO的脱除率由0.55转化为0.75,A到B点NO脱除的物质的量浓度=6×10-4mgm-3×(0.75-0.55)=1.2×10-4mgm-3,该时间段内NO的脱除速率=![]() mgm-3s-1=1.5×10-4mgm-3s-1;
mgm-3s-1=1.5×10-4mgm-3s-1;
(4)根据图知,阴极上进入的离子是HSO3-,出去的离子为S2O42-,电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】常温下向20.00 mL 0.10 mol/L Na2CO3溶液中逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
溶液的pH | 加入盐酸的总体积 |
12 | V(HCl)=0 |
8 | V(HCl)=20.00 mL |
5 | V(HCl)=40.00 mL |
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________(用离子方程式和必要的文字说明)此时溶液中c(H2CO3)____(填“>”、“<”或“=”)c(CO32—)。
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。