题目内容
【题目】某试样含有的阳离子为NH4+、Ag+、Ba2+、Cu2+、Fe2+中的若干种,为确定其组成,某同学进行了如下实验,下列说法不正确的是
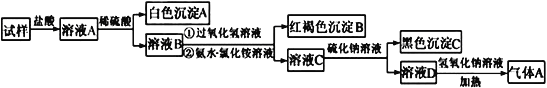
注:①CuS为难溶于水的黑色固体;②气体A能使湿润的红色石蕊试纸变蓝。
A.沉淀A为BaSO4
B.加入过氧化氢溶液时发生的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
C.加入氨水-氯化铵溶液可使Fe3+沉淀完全,而Cu2+不形成沉淀
D.试样中一定含NH4+、Ba2+、Cu2+、Fe2+,一定不含Ag+
【答案】D
【解析】
将试样溶于盐酸,得到溶液A,没有难溶物,所以试样中不存在银离子,向溶液A中加入硫酸,得到白色沉淀A,说明试样中含有钡离,向滤液B中加入强氧化剂(过氧化氢)和氨水-氯化铵溶液,得到红褐色沉淀,说明原溶液中的亚铁离子被氧化为三价铁离子后沉淀下来,向溶液中加入硫化物,得到黑色沉淀,说明原溶液中存在二价铜离子,加入碱液并加热,出现使湿润的红色石蕊试纸变蓝的气体,说明原溶液中存在铵根离子。
A. 沉淀A为BaSO4,A选项正确;
B. 加入过氧化氢溶液时发生的反应:2Fe2++H2O2+2H+=2Fe3++2H2O,B选项正确;
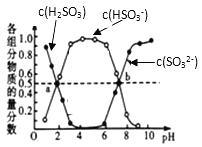
C. 在pH为3左右时,铁离子即可完全沉淀,而铜离子在pH为4.4左右才开始沉淀,所以加入氨水-氯化铵溶液可调节pH,使Fe3+沉淀完全,而Cu2+不形成沉淀,C选项正确;
D. 因为流程中加入了氯化铵,无法确定原溶液是否有铵根离子存在,故D选项错误;
故答案选D。

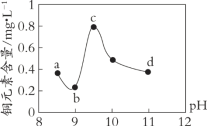
【题目】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
查阅资料,平衡I:Cu(OH)2 + 4NH3 ![]() [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH- ![]() [Cu(OH-)4]2-
[Cu(OH-)4]2-
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/ mg·L-1 | 72 | ≤0.5 |
NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法不正确的是
A. 废水中Cu2+处理的最佳pH约为9
B. b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升
C. c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降
D. d点以后,随c(OH-)增加,铜元素含量可能上升