题目内容
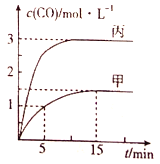
【题目】一定条件下存在反应:C(s)+H2O(g)![]() CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
容器 | 甲 | 乙 | 丙 |
|
容积/L | 1 | 1 | V | |
温度/℃ | T1 | T2 | T1 | |
起始量 | 2 molC(s)、2 mol H2O(g) | 2 mol CO(g)、2 mol H2(g) | 6 molC(s)、 4mol H2O(g) |
下列说法正确的是( )
A.甲容器中,0~5min内的平均反应速率v(CO)=0.1 mol/(L·min)
B.乙容器中,若平衡时n(C)=0.56 mol,则T2>T1
C.温度为T1时,反应的平衡常数为K=9
D.丙容器的容积V=0.8 L
【答案】D
【解析】
A. 甲容器中,0~5min内的平均反应速率v(CO)=![]() =0.2 mol/(L·min),A错误;
=0.2 mol/(L·min),A错误;
B. 乙容器中若平衡时n(C)=0.56 mol,根据方程式知,参加反应的n(C)=n(H2O)=n(H2)=n(CO)=0.56 mol,平衡时c(CO)=c(H2)=![]() =1.44mol/L,c(H2O)=0.56 mol÷1 L=0.56 mol,化学平衡常数K乙=
=1.44mol/L,c(H2O)=0.56 mol÷1 L=0.56 mol,化学平衡常数K乙=![]() ≈3.702,甲容器中达到平衡状态时,c(CO)=c(H2)=1.5 mol/L,c(H2O)=2 mol/L-1.5 mol/L=0.5 mol/L,化学平衡常数K甲=
≈3.702,甲容器中达到平衡状态时,c(CO)=c(H2)=1.5 mol/L,c(H2O)=2 mol/L-1.5 mol/L=0.5 mol/L,化学平衡常数K甲=![]() =4.5,该反应的正反应是吸热反应,升高温度平衡正向移动,化学平衡常数增大,所以K甲大于K乙,说明甲温度高于乙,T2<T1,B错误;
=4.5,该反应的正反应是吸热反应,升高温度平衡正向移动,化学平衡常数增大,所以K甲大于K乙,说明甲温度高于乙,T2<T1,B错误;
C. 根据选项B分析可知,温度为T1时,反应的平衡常数为K=4.5,C错误;
D. 达到平衡状态时,丙中c(CO)=3mol/L,根据方程式可知c(H2)=c(CO)=3 mol/L,温度不变化学平衡常数不变,则平衡时c(H2O)=![]() mol/L=2 mol/L,反应产生的CO的物质的量n(CO)=c·V=3 mol/L×V=3V mol,反应消耗的水的物质的量等于生成的CO的物质的量,所以反应开始时水的物质的量为2V mol+3V mol=4 mol,解得V=0.8 L,D正确;
mol/L=2 mol/L,反应产生的CO的物质的量n(CO)=c·V=3 mol/L×V=3V mol,反应消耗的水的物质的量等于生成的CO的物质的量,所以反应开始时水的物质的量为2V mol+3V mol=4 mol,解得V=0.8 L,D正确;
故合理选项是D。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】已知:反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
k | 1.67 | 1.11 | 1.00 | 0.60 |
下列有关叙述不正确的是
A. 该反应平衡常数表达式为K=[c(CO2)·c(H2)]/[c(CO)·c(H2O)]
B. 该反应的逆反应是吸热反应
C. 830℃时,向恒容密闭容器中加入CO2 和H2各1mol,当测得CO2 的物质的量为0.4mol时,反应处于平衡状态
D. 若某温度下该反应中各物质的平衡浓度符合关系式:[c(CO2)/3c(CO)]=[c(H2O)/5c(H2)],则该温度是1000 C
【题目】某学生用0.1000 mol/L NaOH溶液滴定未知浓度的盐酸溶液,操作可分解为如下几步:
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________。
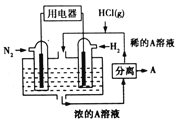
(2)操作F中应该选择图中________滴定管(填标号)。

(3)滴定时边滴边摇动锥形瓶,眼睛应观察________。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是____________________________。
(4)滴定结果如表所示:
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 20 | 1.02 | 21.03 |
2 | 20 | 2.00 | 25.00 |
3 | 20 | 0.60 | 20.60 |
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为________mol/L。
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________(填“是”或“否”)。