题目内容
【题目】下列溶液中微粒的物质的量浓度关系不正确的是![]()
A.若将适量![]() 通入
通入![]()
![]()
![]() 溶液中至溶液恰好呈中性,则溶液中
溶液中至溶液恰好呈中性,则溶液中![]() 不考虑溶液体积变化
不考虑溶液体积变化![]() :2
:2![]()
![]()
![]()
B.某溶液中由水电离出的![]() ,若
,若![]() 时,则该溶液pH一定为
时,则该溶液pH一定为![]()
C.常温下将相同体积的![]() 硫酸和
硫酸和![]() 一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性
一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性
D.等体积等物质的量浓度的NaClO溶液与NaCl溶液中离子总数大小:![]()
【答案】B
【解析】
A、依据反应过程和溶液中存在的电荷守恒分析判断;
B、常温时,某溶液中由水电离出的![]()
![]() ,若
,若![]() 时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液;
时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液;
C、碱的强弱不知,若为强酸、强碱混合,呈中性,若为强酸、弱碱混合,则相同体积的![]() 硫酸和
硫酸和![]() 一元碱BOH溶液混合显碱性;
一元碱BOH溶液混合显碱性;
D、HClO是弱酸,所以NaClO溶液中发生水解反应:![]() ,使溶液呈碱性,氢离子浓度小于
,使溶液呈碱性,氢离子浓度小于![]() ,所以NaCl溶液中
,所以NaCl溶液中![]() 大于NaClO溶液中
大于NaClO溶液中![]() ,依据电荷守恒分析。
,依据电荷守恒分析。
A、将![]() 通入
通入![]()
![]() 溶液中恰好呈中性,溶液中存在电荷守恒,
溶液中恰好呈中性,溶液中存在电荷守恒,![]() ,
,![]() ,则得到
,则得到![]() ,故A正确;
,故A正确;
B.常温时,某溶液中由水电离出的![]()
![]() ,若
,若![]() 时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液,如为酸溶液,则
时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液,如为酸溶液,则![]() ,如为碱溶液,则
,如为碱溶液,则![]() ,故B错误;
,故B错误;
C、![]() 硫酸,
硫酸,![]() ,硫酸完全电离,
,硫酸完全电离,![]() 一元碱BOH,
一元碱BOH,![]() ,若为强酸、强碱混合,混合后溶液呈中性,若为强酸、弱碱混合,氢离子和氢氧根离子正好反应生成盐和水,而弱碱存在电离平衡,平衡右移,还可以继续电离出氢氧根离子,所以溶液呈碱性,故C正确;
,若为强酸、强碱混合,混合后溶液呈中性,若为强酸、弱碱混合,氢离子和氢氧根离子正好反应生成盐和水,而弱碱存在电离平衡,平衡右移,还可以继续电离出氢氧根离子,所以溶液呈碱性,故C正确;
D、HClO是弱酸,所以NaClO溶液中发生水解反应:![]() ,使溶液呈碱性,氢离子浓度小于
,使溶液呈碱性,氢离子浓度小于![]() ,所以NaCl溶液中
,所以NaCl溶液中![]() 大于NaClO溶液中
大于NaClO溶液中![]() ,根据电荷守恒:
,根据电荷守恒:![]() 可得溶液中离子总数为
可得溶液中离子总数为![]() ;同理可得NaClO溶液中总数为
;同理可得NaClO溶液中总数为![]() ,所以NaCl溶液中离子总数大于NaClO溶液,故D正确;
,所以NaCl溶液中离子总数大于NaClO溶液,故D正确;
故选:B。

【题目】石油资源紧张曾是制约中国发展轿车事业,尤其是制约轿车进入家庭的重要因素。据报道,中国宣布将推广“车用乙醇汽油”。
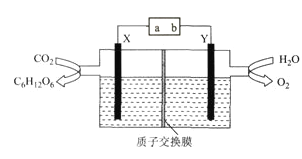
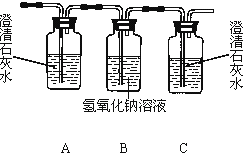
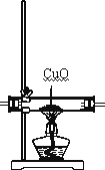
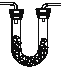
(1)乙醇燃烧时如果氧气不足,可能还有CO生成.用下图装置正确验证乙醇燃烧产物有CO、![]() 、
、![]() ,应将乙醇燃烧产物依次通过,按气流从左至右顺序填装置编号______。
,应将乙醇燃烧产物依次通过,按气流从左至右顺序填装置编号______。
编号 | ① | ② | ③ | ④ |
装置 |
|
|
|
|
(2)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是______;B瓶溶液的作用是______。
(3)装置①中所盛的是______溶液,证明燃烧产物中含有CO的实验现象是:______。
(4)装置④中所盛的固体药品是______,它可以验证的产物是______。
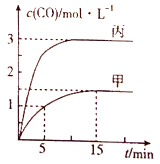
【题目】一定条件下存在反应:C(s)+H2O(g)![]() CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
容器 | 甲 | 乙 | 丙 |
|
容积/L | 1 | 1 | V | |
温度/℃ | T1 | T2 | T1 | |
起始量 | 2 molC(s)、2 mol H2O(g) | 2 mol CO(g)、2 mol H2(g) | 6 molC(s)、 4mol H2O(g) |
下列说法正确的是( )
A.甲容器中,0~5min内的平均反应速率v(CO)=0.1 mol/(L·min)
B.乙容器中,若平衡时n(C)=0.56 mol,则T2>T1
C.温度为T1时,反应的平衡常数为K=9
D.丙容器的容积V=0.8 L