题目内容
下列说法正确的是
| A.欲配制1.00L 1.00mol·L-1的NaCI溶液,可将58.5g NaC1溶于1.00L水中 |
| B.0.1mol Na2O2与足量水反应,转移电子数为0.2NA |
| C.同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 |
| D.1.0L 1.0mol ·L-l的NaAlO2水溶液中含有的氧原子数大于2NA |
D
解析试题分析:A项中水的体积为1.00L,溶液的体积不确定,错误;B项根据方程式确定0.1molNa2O2反应式转移的电子数为0.1 NA,错误;C项中两者的体积比与物质的量之比相等,均为11:16,错误;D项考虑溶液中水所含的氧原子,正确。
考点:阿伏伽德罗常数。

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.107克Fe(OH)3胶体中,含有的胶粒数目为NA |
| B.46克NO2和N2O4的混合物中,含有原子的数目为3NA |
| C.标准状况下,2.24L的Cl2溶于水中达到饱和,转移的电子数目为0.1NA |
| D.2.3克Na与O2完全反应,反应中转移的电子数目介于0.1NA与0.2NA之间 |
下列说法正确的是( )
| A.1L1mol?L-1的NH4Cl溶液中一定含有NA个NH4+ |
| B.常温常压下,22.4L乙烯中含共价键数为5 NA |
| C.6.8g熔融的KHSO4中含有0.05 NA个阳离子 |
| D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下反应可生成NA个H2O |
用NA表示阿伏加德罗数,下列叙述正确的是( )
| A.7.8gNa2O2固体中阴、阳离子数之和一定为0.3NA |
| B.室温下,14.0g乙烯和丁烯的混合气体中含有的氢原子数目为NA |
| C.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| D.常温常压下,1mol甲基所含的电子总数为7 NA |
NA为阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,5.6 L氯气和16.8 L氧气的混合气体中含有分子数为NA |
| B.标准状况下,22.4 LH2O所含有原子数为3NA |
| C.NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D.1 mol Na2O2与H2O完全反应,转移2NA个电子 |
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是 ( )。
| A.该原子的摩尔质量是aNA g |
B.W g该原子的物质的量一定是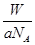 mol mol |
C.W g该原子中含有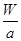 ×NA个该原子 ×NA个该原子 |
D.由已知信息可得:NA=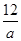 |
某溶液中大量存在以下浓度的五种离子:0.2 mol·L-1 Cl-、0.4 mol·L-1 SO42-、0.1 mol·L-1 Al3+、0.3 mol·L-1 H+、M,则M及其物质的量浓度可能为( )。
| A.Na+ 0.3 mol·L-1 | B.Zn2+ 0.2 mol·L-1 |
| C.CO32- 0.2 mol·L-1 | D.Ca2+ 0.1 mol·L-1 |
把一块镁铝合金投入到1 mol/L盐酸里,待合金完全溶解后,往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图A所示。下列说法中不正确的是( )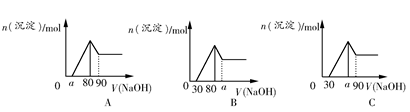
| A.a的取值范围为0≤a<50 |
B.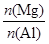 的最大值为2.5 的最大值为2.5 |
| C.若将关系图改为图B,则a的取值范围为80<a<90 |
| D.若将关系图改为图C,则a的取值范围为75<a<90 |
用8 mol·L-1的磷酸溶液和氨气配制一种培养液,要使此溶液中NH4H2PO4和(NH4)2HPO4的物质的量之比为3∶1,每升溶液中含磷元素0.1 mol,现要配制4 L这种溶液,需标况下的氨气的体积为 ( )。
| A.2.8 L | B.5.6 L | C.11.2 L | D.22.4 L |