题目内容
NA为阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,5.6 L氯气和16.8 L氧气的混合气体中含有分子数为NA |
| B.标准状况下,22.4 LH2O所含有原子数为3NA |
| C.NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D.1 mol Na2O2与H2O完全反应,转移2NA个电子 |
A
解析试题分析:A、根据阿伏伽德罗定律级推论,标准状况下,22.4L的任何气体(包括混合气体)的物质的量都为1mol,分子数为NA,正确;B、标准状况时,水不为气体,无法计算其物质的量,错误;C、气体的物质的量之比,不一定等于体积之比,未指明同温同压条件,错误;D、Na2O2既是氧化剂又是还原剂,所以1 mol Na2O2与H2O完全反应,转移NA个电子,错误,答案选A。
考点:考查对阿伏伽德罗常数的理解

练习册系列答案
相关题目
下列说法正确的是
| A.欲配制1.00L 1.00mol·L-1的NaCI溶液,可将58.5g NaC1溶于1.00L水中 |
| B.0.1mol Na2O2与足量水反应,转移电子数为0.2NA |
| C.同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 |
| D.1.0L 1.0mol ·L-l的NaAlO2水溶液中含有的氧原子数大于2NA |
设NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1L 0.1 mol·L—1的CH3COONa溶液中CH3COO—的总数是0.1NA |
| B.常温常压下,1.6g O2和O3混合气体中质子总数为0.8 NA |
| C.一定条件下,2mol SO2和 1mol O2发生反应,转移的电子总数一定是4NA |
| D.1L 0.1mol·L—1的葡萄糖溶液中分子总数为0.1 NA |
NA为阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,11.2L的己烷所含的分子数为0.5NA个 |
| B.28g乙烯所含共用电子对数目为4NA个 |
| C.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA个 |
| D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA个 |
下列有关化学用语的表示正确的是( )
A.NH4Br的电子式: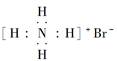 |
B.S2-的结构示意图: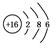 |
C.原子核内有18个中子的氯分子: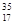 Cl2 Cl2 |
| D.CS2分子的结构式:S—C—S |
下列叙述中正确的是( )
| A.相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 |
| B.标准状况下,28 g CO和22.4 L SO3所含分子数相等 |
| C.5.6 g铁粉与足量氯气充分反应,有0.2 mol电子转移 |
| D.等物质的量的CH5+和NH2—所含电子数相等 |
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )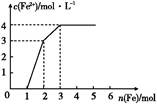
| A.1∶1∶1 | B.1∶3∶1 | C.3∶3∶8 | D.1∶1∶4 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.在1 L 0.1 mol/L硫化钠溶液中阴离子总数大于0.1NA |
| B.1 mol O2作氧化剂时转移电子数一定为4NA |
| C.标准状况下,22.4 L戊烷所含分子数为NA |
| D.在1 L 1.0 mol/L NaCl溶液中含有NA个NaCl分子 |