题目内容
7.设nA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温下,46g NO2和N2O4含有2nA个氧原子 | |
| B. | 1mol Na在空气中燃烧,转移2nA个电子 | |
| C. | 1L0.1mol•L-1CH3COOH溶液中含有0.1nA个H+ | |
| D. | 标况下,22.4LHF中含有nA个HF分子 |
分析 A、NO2和N2O4的最简式均为NO2;
B、根据反应后钠元素的化合价变为+1价来分析;
C、醋酸是弱电解质,不能完全电离;
D、标况下,HF为液体.
解答 解:A、NO2和N2O4的最简式均为NO2,故46g混合气体中含有的NO2的物质的量n=$\frac{46g}{46g/mol}$=1mol,则由于2mol氧原子,即2nA个,故A正确;
B、反应后钠元素的化合价变为+1价,故1mol钠失去1mol电子,即nA个,故B错误;
C、醋酸是弱电解质,不能完全电离,故溶液中的氢离子的个数小于0.1nA个,故C错误;
D、标况下,HF为液体,不能根据气体摩尔体积来计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的应用,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.下列有关物质性质和应用正确的是( )
| A. | 甲醛能使蛋白质变性,可用于食品防腐剂 | |
| B. | 炭具有还原性,一定条件下能将二氧化硅还原为硅 | |
| C. | 硅酸钠溶液呈碱性,常用作木材的防火剂 | |
| D. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 |
2.如图所示,常温时将一滴管液体Y一次性全部挤到充满O2的锥形瓶内(装置气密性良好),若锥形瓶内气体的最大物质的量是amol,久置后其气体的物质的量是bmol,不存在a>b关系的是( )
| X | Y | 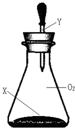 | |
| A | 过量C、Fe碎屑 | 稀HCl | |
| B | 过量Na2CO3粉末 | 稀H2SO4 | |
| C | 过量Fe、Al碎屑 | 浓H2SO4 | |
| D | 过量Cu、CuO粉末 | 浓HNO3 |
| A. | A | B. | B | C. | C | D. | D |
12.某同学对下列四个实验都设计了两种方案,其中两种方案均合理的是( )
| 选项 | A | B | C | D |
| 实验目的 | 清洗铁制品表面的铁锈 | 除去碳酸钠中少量的碳酸氢钠 | 鉴别二氧化氮和溴蒸气 | 检验二氧化碳中含有少量的二氧化硫 |
| 方案1 | 加适量稀盐酸 | 溶解后加盐酸 | 加水 | 通入品红溶液 |
| 方案2 | 用水洗涤 | 加热 | 加硝酸银溶液 | 通入澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
19.只运用物理方法就能从海水中获得的物质是( )
| A. | I2 | B. | Br2 | C. | Mg | D. | NaCl |
16.下列各组离子中,能在溶液中大量共存的是( )
| A. | Na+,OH-,K+,SO42- | B. | Ag+,K+,NO3-,CO32- | ||
| C. | K+,Cu2+,OH-,Cl- | D. | Na+,Ba2+,SO42-,Cl- |
17.NF3气体可由氨气和氟气反应得到:4NH3+3F2═NF3+3NH4F.下列有关说法中正确的是( )
| A. | 该反应前后氮元素的化合价不变 | |
| B. | 该反应中的四种物质晶体中都存在氢键 | |
| C. | 该反应中NH3、F2、NF3的分子中所有原子均共平面 | |
| D. | 该反应中NH3、F2、NF3三种物质的晶体均属于分子晶体 |