题目内容
【题目】下列各组粒子,属于同种核素的是_____(填编号,下同),互为同位素的是______,互为同素异形体的是_____,属于同种物质的是_________。
①16O2和18O3②16O2和18O2③ H、D、T ④![]() 和
和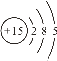 (核内15个中子)
(核内15个中子)
【答案】④ ③ ① ②
【解析】
核素是指具有一定数目质子和一定数目中子的原子,同种核素即质子数、中子数分别相同的核素;具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;同素异形体是同种元素形成的不同单质;分子式相同、结构也相同的物质属于同种物质。
①16O2和18O3 是同种元素形成的不同单质,互为同素异形体;
②16O2和18O2是同种元素形成的同种单质,属于同种物质;
③H、D、T的质子数都为1,中子数分别为0、1、2,属于质子数相同、中子数不同的氢元素的不同核素,互为同位素;
④![]() 和
和  (核内15个中子)的质子数都为15,中子数都为15,是两种质子数、中子数分别相同的核素,属于同种核素;
(核内15个中子)的质子数都为15,中子数都为15,是两种质子数、中子数分别相同的核素,属于同种核素;
综上,属于同种核素的是④,互为同位素的是③,互为同素异形体的是①,属于同种物质的是②,答案为:④;③;①;②。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目