��Ŀ����
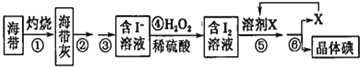
����Ŀ����������dz��õ���������ij��ѧС����ʵ���������̿�(��Ҫ�ɷ���MnO2)Ϊԭ���Ʊ�KMnO4����ͼ��ʵ�����Ʊ�������صIJ������̡�

��֪��
�¶� | �ܽ��/g | ||
K2CO3 | KHCO3 | KMnO4 | |
20�� | 111 | 33.7 | 6.38 |
��ش�
(1) ��Ӧ�ٵĻ�ѧ����ʽΪ______________________________________���������̿�KClO3��KOH���壬�����żܡ��������������Ǻ��������⣬���õ���������___�������ô�������ѡ����������������______________
(2) ��Ӧ�������������뻹ԭ��������ʵ���֮��Ϊ___________________�����������п���ѭ�����õ�������__________________________��
(3) ʵ��ʱ������Һ�еõ�KMnO4�����ʵ�����aΪ___________________����CO2����������KHCO3�����µõ���KMnO4��Ʒ�Ĵ��Ƚ�����ԭ����________��
���𰸡�(1) KClO3 + 3MnO2 + 6KOH![]() 3K2MnO4 + KCl + 3H2O �ƾ��ơ�����ǯ �������е�SiO2����KOH������Ӧ 2:1 KOH��MnO2 ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����� KHCO3���ܽ�Ƚ�С����Һ����Ũ�����½ᾧʱKHCO3����KMnO4һͬ�ᾧ����
3K2MnO4 + KCl + 3H2O �ƾ��ơ�����ǯ �������е�SiO2����KOH������Ӧ 2:1 KOH��MnO2 ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����� KHCO3���ܽ�Ƚ�С����Һ����Ũ�����½ᾧʱKHCO3����KMnO4һͬ�ᾧ����
��������
�����̿���Ҫ�ɷ���MnO2��Ϊԭ���Ʊ�KMnO4���壬���̿�����KOH�������������������գ��õ�ī��ɫ�ۿ飬ΪK2MnO4����ȴ������ˮ��ˮ��Һ������ɫ������������ڼ���Һ�е�������ɫ�����ȱ�ͨ������������̼���壬������ҺpH���ȹ��˵õ�MnO2��KMnO4��Һ����ȴ�ᾧ�õ�KMnO4���塣�ż��������£�MnO2��KOH��KClO3��Ӧ����K2MnO4��KCl��H2O�����ڹ���������Ҫ�������ڼ��ȣ����������ﺬ�м�������KOHӦ�������������������еĶ��������ǿ�Ӧ����������ʴ���ƹ������̿�֪��CO2ʹMnO42-�����绯��Ӧ������MnO4-��MnO2������Ԫ���غ��֪��������K2CO3����ͨ��CO2̫�࣬����KHCO3���ɣ���Һ�к���KHCO3��KMnO4��������ԭ��Ӧ�е���������Ԫ�ػ��ϼ۽��͵����ʣ���ԭ����Ԫ�ػ��ϼ����ߵ����ʣ���ϻ�ѧ����ʽ������ϵ�͵����غ���㣻��������Ҫ����������ں��������ɸ����ʣ������ʿ���ѭ�����ã��Ǵ���Һ�еõ����ʵķ�����Ũ����������ȴ�ᾧ�����˻���˵õ����壻�������̿�֪��������̼ʹMnO42-�����绯��Ӧ������MnO4-��MnO2������Ԫ���غ��֪��������K2CO3����ͨ�������̼̫�࣬����KHCO3���ɣ���Һ�к���KHCO3��������أ�
(1).���������£�MnO2��KOH��KClO3��Ӧ����K2MnO4��KCl��H2O����Ӧ�Ļ�ѧ����ʽΪ3MnO2��KClO3��6KOH![]() 3K2MnO4��KCl��3H2O���������̿�KClO3��KOH��������ʱ������KOH����������е�SiO2������Ӧ��2KOH+SiO2
3K2MnO4��KCl��3H2O���������̿�KClO3��KOH��������ʱ������KOH����������е�SiO2������Ӧ��2KOH+SiO2![]() K2SiO3+H2O��ʴ������������Fe������Ӧ������Ҫ����������
K2SiO3+H2O��ʴ������������Fe������Ӧ������Ҫ����������
�ʴ�ΪKClO3 + 3MnO2 + 6KOH![]() 3K2MnO4 + KCl + 3H2O���ƾ��ơ�����ǯ���������е�SiO2����KOH������Ӧ��
3K2MnO4 + KCl + 3H2O���ƾ��ơ�����ǯ���������е�SiO2����KOH������Ӧ��
(2).������ͼ��֪��������̼ʹMnO42-�����绯��Ӧ������MnO4-��MnO2������Ԫ���غ��֪��������K2CO3����ͨ�������̼̫�࣬����KHCO3���ɣ���Һ�к���KHCO3��KMnO4���ڼ���Ũ��ʱ������KHCO3��KMnO4����һ��������ʵ����ͨ������������̼ʱ��ϵ�п��ܷ�����Ӧ�����ӷ���ʽΪ��3MnO42-+2CO2=2 MnO4-+MnO2��+2CO32-��2OH-+ CO2=CO32-+ H2O������������ԭ��Ӧ���������ͻ�ԭ������KMnO4�������������ͻ�ԭ���������ȼ�Ϊ��Ӧ�����ʵ���֮��Ϊ1:2��������ҺpH�����У��������������뻹ԭ��������ʵ���֮��Ϊ2:1��������ͼ���Կ�������Ҫ�����������MnO2��KOH��KClO3��CO2��ˮ���Բ����ǣ�����Ӧ��������KOH�� MnO2����KOH�� MnO2�ǿ���ѭ�����õ����ʣ��ʴ�Ϊ��2:1��KOH�� MnO2��
(3).���������е���Ϣ����Һ�к��д����ĸ�����غ�̼��أ��ٸ��ݱ��е��ܽ�����ݿ�֪����������������µ��ܽ�Ƚ�С����̼��ص��ܽ�Ⱥܴ���ˣ�����Һ�еõ�KMnO4�����ʵ�������Ũ����������ȴ�ᾧ�����˻���˵õ����壻�������̿�֪��������̼ʹMnO42-�����绯��Ӧ������MnO4-��MnO2������Ԫ���غ��֪��������K2CO3����ͨ�������̼̫�࣬����KHCO3���ɣ���Һ�к���KHCO3��KMnO4���ڼ���Ũ��ʱ������KHCO3��KMnO4����һ���������ʴ�Ϊ������Ũ������ȴ�ᾧ�����ˣ�KHCO3���ܽ�ȱ�K2CO3С�ö࣬��Һ����Ũ��ʱKHCO3����KMnO4һ��ᾧ������

 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�